Penerbitan baru
Sistem penyampaian ubat gelung tertutup boleh meningkatkan rawatan kemoterapi
Ulasan terakhir: 02.07.2025

Semua kandungan iLive disemak secara perubatan atau fakta diperiksa untuk memastikan ketepatan faktual sebanyak mungkin.
Kami mempunyai garis panduan sumber yang ketat dan hanya memautkan ke tapak media yang bereputasi, institusi penyelidikan akademik dan, apabila mungkin, dikaji semula kajian secara medis. Perhatikan bahawa nombor dalam kurungan ([1], [2], dan lain-lain) boleh diklik pautan ke kajian ini.
Jika anda merasakan bahawa mana-mana kandungan kami tidak tepat, ketinggalan zaman, atau tidak dipersoalkan, sila pilih dan tekan Ctrl + Enter.
Apabila pesakit kanser menjalani kemoterapi, dos kebanyakan ubat dikira berdasarkan luas permukaan badan pesakit. Ini dianggarkan menggunakan persamaan yang mengambil kira ketinggian dan berat pesakit. Persamaan ini telah dirumuskan pada tahun 1916 berdasarkan data daripada hanya sembilan pesakit.
Pendekatan dos yang dipermudahkan ini tidak mengambil kira faktor lain dan mungkin menyebabkan pesakit diberi terlalu banyak atau terlalu sedikit ubat. Akibatnya, sesetengah pesakit mungkin mengalami ketoksikan yang tidak perlu atau keberkesanan yang tidak mencukupi daripada kemoterapi yang mereka terima.
Untuk meningkatkan ketepatan dos kemoterapi, jurutera MIT telah membangunkan pendekatan alternatif yang membolehkan dos diperibadikan untuk setiap pesakit. Sistem mereka mengukur jumlah ubat dalam badan pesakit dan menyuapkan data tersebut ke dalam pengawal yang boleh melaraskan kadar infusi dengan sewajarnya.
Pendekatan ini boleh membantu mengimbangi perbezaan dalam farmakokinetik ubat yang disebabkan oleh komposisi badan, kecenderungan genetik, ketoksikan organ yang disebabkan oleh kemoterapi, interaksi dengan ubat dan makanan lain, dan variasi sirkadian dalam enzim yang bertanggungjawab untuk memecahkan ubat kemoterapi, kata para penyelidik.
"Dengan mengiktiraf kemajuan dalam memahami cara ubat dimetabolismekan dan menggunakan alat kejuruteraan untuk memudahkan dos yang diperibadikan, kami percaya kami boleh membantu mengubah keselamatan dan keberkesanan banyak ubat," kata Giovanni Traverso, profesor kejuruteraan mekanikal bersekutu di MIT, ahli gastroenterologi di Brigham and Women's Hospital, dan pengarang kanan kajian itu.
Louis DeRidder, pelajar siswazah di MIT, adalah pengarang utama kertas kerja yang diterbitkan dalam jurnal Med.
Pemantauan berterusan
Dalam kajian ini, para penyelidik memberi tumpuan kepada ubat yang dipanggil 5-fluorouracil, yang digunakan untuk merawat kanser kolorektal dan kanser lain. Ubat ini biasanya diberikan dalam tempoh 46 jam, dan dosnya ditentukan menggunakan formula berdasarkan ketinggian dan berat pesakit, yang memberikan anggaran luas permukaan badan.
Walau bagaimanapun, pendekatan ini tidak mengambil kira perbezaan dalam komposisi badan yang boleh menjejaskan cara ubat itu diedarkan dalam badan, atau variasi genetik yang mempengaruhi cara ia dimetabolismekan. Perbezaan ini boleh membawa kepada kesan sampingan yang berbahaya jika terlalu banyak ubat diberikan. Jika tidak cukup ubat yang diberikan, ia mungkin tidak membunuh tumor seperti yang diharapkan.
"Orang yang mempunyai luas permukaan badan yang sama boleh mempunyai ketinggian dan berat yang sangat berbeza, jisim otot yang berbeza, atau genetik yang berbeza, tetapi selagi ketinggian dan berat yang dimasukkan ke dalam persamaan itu menghasilkan kawasan permukaan badan yang sama, dos mereka adalah sama, " kata DeRidder, calon PhD dalam program kejuruteraan perubatan dan fizik perubatan di Program Harvard-MIT dalam Sains dan Teknologi Kesihatan.
Faktor lain yang boleh mengubah jumlah ubat dalam darah pada bila-bila masa ialah variasi sirkadian dalam enzim yang dipanggil dihydropyrimidine dehydrogenase (DPD), yang memecahkan 5-fluorouracil. Ekspresi DPD, seperti banyak enzim lain dalam badan, dikawal oleh irama sirkadian. Oleh itu, degradasi 5-FU oleh DPD tidak tetap, tetapi berbeza mengikut masa hari. Irama sirkadian ini boleh menghasilkan variasi sepuluh kali ganda dalam jumlah 5-FU dalam darah pesakit semasa infusi.
"Dengan menggunakan kawasan permukaan badan untuk mengira dos kemoterapi, kami tahu bahawa dua orang boleh mempunyai ketoksikan yang sangat berbeza daripada 5-fluorouracil. Seorang pesakit boleh menjalani kitaran rawatan dengan ketoksikan yang minimum, dan kemudian kitaran dengan ketoksikan yang teruk. Sesuatu telah berubah dalam cara pesakit memetabolismekan kemoterapi daripada satu kitaran ke kitaran seterusnya. Kaedah dos kami yang lapuk mengatakan bahawa pesakit tidak mengalami perubahan ini, dan seorang pakar Rubinson, dan seorang pakar klinikal Douglas. Institut Kanser Dana-Farber dan pengarang kertas itu.
Satu cara untuk cuba mengimbangi kebolehubahan dalam farmakokinetik kemoterapi ialah strategi yang dipanggil pemantauan ubat terapeutik, di mana pesakit memberikan sampel darah pada akhir satu kitaran rawatan. Selepas sampel ini dianalisis untuk kepekatan ubat, dos boleh diselaraskan, jika perlu, pada permulaan kitaran seterusnya (biasanya dua minggu untuk 5-fluorouracil).
Pendekatan ini telah ditunjukkan untuk membawa kepada hasil yang lebih baik untuk pesakit, tetapi tidak digunakan secara meluas untuk kemoterapi seperti 5-fluorouracil.
Penyelidik MIT ingin membangunkan jenis pemantauan yang serupa, tetapi dengan cara automatik yang membolehkan dos ubat diperibadikan dalam masa nyata, yang boleh membawa kepada hasil yang lebih baik untuk pesakit.
Dalam sistem gelung tertutup mereka, kepekatan ubat boleh dipantau secara berterusan dan maklumat ini digunakan untuk melaraskan secara automatik kadar infusi ubat kemoterapi untuk mengekalkan dos dalam julat sasaran.
Sistem gelung tertutup ini membolehkan dos ubat diperibadikan untuk mengambil kira irama sirkadian tahap enzim metabolisme dadah, serta sebarang perubahan dalam farmakokinetik pesakit sejak rawatan terakhir, seperti ketoksikan organ yang disebabkan oleh kemoterapi.
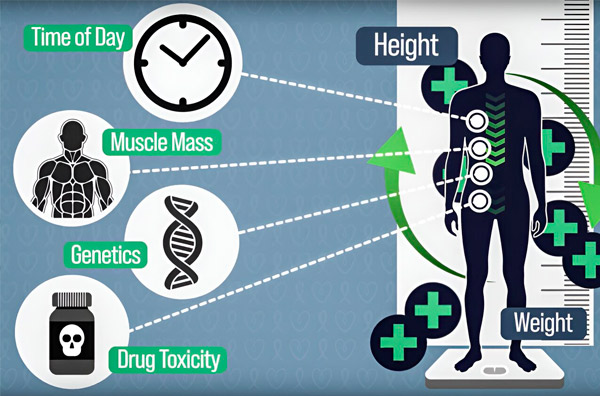
Untuk menjadikan dos kemoterapi lebih tepat, jurutera MIT telah membangunkan cara untuk terus mengukur jumlah ubat dalam badan pesakit semasa infusi berbilang jam. Ini akan membantu mengimbangi perbezaan yang disebabkan oleh komposisi badan, genetik, ketoksikan dadah dan ayunan sirkadian. Sumber: Ihsan penyelidik.
Sistem baharu yang dibangunkan oleh penyelidik, dikenali sebagai CLAUDIA (RegulAtor Infus Dadah Automatik Gelung Tertutup), menggunakan peralatan yang tersedia secara komersial untuk setiap langkah. Sampel darah diambil setiap lima minit dan cepat disediakan untuk analisis. Kepekatan 5-fluorouracil dalam darah diukur dan dibandingkan dengan julat sasaran.
Perbezaan antara sasaran dan kepekatan yang diukur dimasukkan ke dalam algoritma kawalan, yang kemudiannya melaraskan kadar infusi yang perlu untuk mengekalkan dos dalam julat kepekatan di mana ubat itu berkesan dan tidak toksik.
"Kami telah membangunkan sistem di mana kami boleh terus mengukur kepekatan ubat dan menyesuaikan kadar infusi dengan sewajarnya untuk mengekalkan kepekatan ubat dalam tetingkap terapeutik, " kata DeRidder.
Pelarasan pantas
Dalam ujian haiwan, para penyelidik mendapati bahawa menggunakan CLAUDIA mereka boleh mengekalkan jumlah ubat yang beredar di dalam badan dalam julat sasaran kira-kira 45 peratus pada masa itu.
Tahap ubat dalam haiwan yang diberi kemoterapi tanpa CLAUDIA kekal dalam julat sasaran hanya 13 peratus daripada masa secara purata. Para penyelidik tidak menguji keberkesanan tahap ubat dalam kajian ini, tetapi mengekalkan kepekatan dalam tetingkap sasaran dianggap menghasilkan hasil yang lebih baik dan kurang ketoksikan.
CLAUDIA juga dapat mengekalkan dos 5-fluorourasil dalam julat sasaran walaupun apabila ubat yang menghalang enzim DPD diberikan. Pada haiwan yang diberi perencat ini tanpa pemantauan dan pelarasan berterusan, paras 5-fluorourasil meningkat sehingga lapan kali ganda.
Untuk demonstrasi ini, penyelidik secara manual melakukan setiap langkah proses menggunakan peralatan luar, tetapi kini merancang untuk mengautomasikan setiap langkah supaya pemantauan dan pelarasan dos boleh dilakukan tanpa campur tangan manusia.
Untuk mengukur kepekatan ubat, para penyelidik menggunakan spektrometri jisim kromatografi cecair berprestasi tinggi (HPLC-MS), teknik yang boleh disesuaikan untuk mengesan hampir semua jenis ubat.
"Kami melihat masa depan di mana kami boleh menggunakan CLAUDIA untuk mana-mana ubat yang mempunyai sifat farmakokinetik yang sesuai dan boleh dikesan oleh HPLC-MS, membenarkan dos yang diperibadikan untuk banyak ubat yang berbeza," kata DeRidder.
