Pakar perubatan artikel itu
Penerbitan baru
Glioma otak
Last reviewed: 29.06.2025

Semua kandungan iLive disemak secara perubatan atau fakta diperiksa untuk memastikan ketepatan faktual sebanyak mungkin.
Kami mempunyai garis panduan sumber yang ketat dan hanya memautkan ke tapak media yang bereputasi, institusi penyelidikan akademik dan, apabila mungkin, dikaji semula kajian secara medis. Perhatikan bahawa nombor dalam kurungan ([1], [2], dan lain-lain) boleh diklik pautan ke kajian ini.
Jika anda merasakan bahawa mana-mana kandungan kami tidak tepat, ketinggalan zaman, atau tidak dipersoalkan, sila pilih dan tekan Ctrl + Enter.
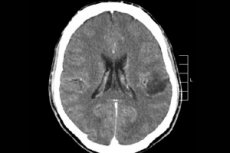
Di antara banyak proses tumor sistem saraf pusat, glioma otak paling kerap didiagnosis - istilah ini adalah kolektif, neoplasma menggabungkan semua fokus oligodendroglial dan astrocytic yang tersebar, astrocytoma, astroblastoma dan sebagainya. Tumor sedemikian boleh mempunyai tahap keganasan yang berbeza, terbentuk daripada struktur glial - sel yang disetempat di sekeliling neuron. Kawasan utama lokasi glioma adalah hemisfera serebrum, dinding ventrikel otak dan chiasma - kawasan persimpangan separa gentian saraf optik. Secara luaran, tumor adalah unsur nodular warna merah jambu atau kemerahan, konfigurasi berbentuk bulat atau gelendong dengan sempadan yang tidak jelas. [ 1 ]
Epidemiologi
Dalam kira-kira 5% kes, glioma dikaitkan dengan patologi keturunan - khususnya, neurofibromatosis dan sindrom lain dengan warisan dominan. Pakar menunjukkan bahawa majoriti mutlak glioma otak berkembang secara sporadis - iaitu, tanpa sebab yang jelas.
Secara keseluruhannya, neoplasma utama sistem saraf pusat menyumbang kira-kira 2% daripada semua tumor, atau lebih daripada 21 kes bagi setiap seratus ribu penduduk. Antaranya, glioma berlaku dalam 35-36% kes, dan lebih daripada 15% daripadanya adalah glioblastoma.
Menurut beberapa data, glioma memberi kesan kepada lelaki lebih kerap berbanding wanita - tumor adalah biasa di kalangan orang yang berumur lebih dari 50 tahun.
Insiden global glioma di kalangan warga tua telah meningkat dengan ketara dalam beberapa dekad kebelakangan ini. Sebab-sebab fenomena ini masih belum ditubuhkan.
Menurut definisi Pertubuhan Kesihatan Sedunia, tiga varian utama tumor glial, berbeza dalam ciri histologinya, telah dikenal pasti. Ini adalah oligodendrogliomas, astrocytomas dan oligoastrocytomas gabungan. Insiden setiap subtipe patologi malignan rendah belum dapat ditentukan dengan pasti. Sesetengah kajian menunjukkan peningkatan dalam kejadian oligodendroglioma daripada 5% kepada 30% dan penurunan dalam kejadian astrocytomas.
Tumor glial mampu menyusup ke tisu otak, dan sebahagian besar fokus gred rendah menjadi malignan dalam masa beberapa tahun. [ 2 ]
Punca daripada glioma otak
Glioma otak adalah keseluruhan kumpulan proses tumor, ciri umumnya ialah pembentukannya daripada struktur glial CNS yang terletak di dalam tisu otak. Tumor sedemikian dibahagikan kepada dua varian histopatologi: glioma malignan tinggi dan malignan rendah.
Sumber pembentukan pertumbuhan adalah sel neuroglia (astrocytes, oligodendrocytes), yang menyediakan asas struktur dan daya maju neuron otak.
Proses tumor glial sangat berbeza dalam struktur, perubahan mutasi dalam gen, keagresifan, ciri klinikal, ciri diagnostik, tindak balas terhadap rawatan, dan prognosis pesakit. Neoplasma embrio dan ependymal sistem saraf pusat - khususnya, medulloblastoma dan ependymomas - berbeza dalam struktur histologinya tetapi serupa dari segi rawatan.
Unsur glial pertama kali diklasifikasikan sebagai kategori struktur berasingan sistem saraf pada akhir abad ke-19.
Tisu neuroglia terdiri daripada sel-sel yang mempunyai fungsi tambahan: trofik, sokongan, pelindung, penyembunyian. Neuron dan gliosit wujud bersama-sama antara satu sama lain, mereka bersama-sama membentuk sistem saraf dan sangat penting dalam proses umum aktiviti penting organisma.
Gliosit secara kasarnya dikategorikan kepada beberapa bentuk utama: astrocytes, oligodendrocytes, sel ependymal, dan microglia.
Sehingga kini, saintis tidak dapat menjawab soalan mengenai punca yang boleh dipercayai pembentukan tumor neuroglial. Agaknya, sumbangan negatif tertentu dibuat oleh kesan radioaktif, penyakit berjangkit, mabuk (terutamanya kimia, pekerjaan). Faktor keturunan juga penting.
Glioma otak timbul daripada neurogliosit yang tidak normal yang mempunyai kecacatan genetik yang membawa kepada pertumbuhan dan fungsi yang tidak normal - struktur tersebut dirujuk sebagai "tidak matang". Sel-sel yang tidak lengkap lebih kerap terletak di satu kawasan, di mana tumor terbentuk.
Ringkasnya, pembentukan glial adalah hasil daripada pertumbuhan sel neuroglia yang diubah suai yang huru-hara dan sporadis. Proses ini boleh berkembang daripada ependymocytes, oligodendrocytes, astrocytes (astrocytoma, termasuk sel gergasi dan anaplastik). [ 3 ]
Faktor-faktor risiko
Walaupun pakar tidak dapat mencirikan dengan tepat punca pembentukan onkopatologi glial, dalam beberapa kes penampilan mereka dapat dicegah dengan menghapuskan faktor risiko utama:
- Pendedahan sinaran mengion mempunyai aktiviti karsinogenik, boleh menyebabkan perkembangan leukemia dan pembentukan proses kanser dengan struktur yang padat, termasuk pada orang yang berumur muda. Prosedur perubatan radiologi yang kerap dan tidak munasabah, sinaran ultraungu (termasuk solarium) juga tergolong dalam kesan karsinogenik yang berpotensi dan boleh menyebabkan kemunculan tumor dalam pelbagai organ, termasuk otak.
- Kesan buruk pekerjaan, mabuk sering mempunyai hubungan kausal dengan perkembangan tumor kanser. Pengeluaran getah dan kaca, racun perosak dan bahan api, logam dan tekstil, cat dan reagen makmal dianggap sangat berbahaya. Berisiko ialah pekerja dalam industri aeroangkasa, arang batu dan logam, kilang pembuatan kimia dan produk sampingan, bahan binaan dan elektrod, bahan api dan pelincir, plastik dan monomer.
- Pencemaran udara, air dan tanah bertanggungjawab untuk sehingga 4% daripada semua patologi kanser di dunia. Karsinogen, terdapat dalam kuantiti yang banyak dalam persekitaran, memasuki badan dengan udara yang disedut, air minuman dan makanan. Tinggal di kawasan yang tidak selamat dari segi ekologi - berhampiran kemudahan perindustrian yang besar, persimpangan pengangkutan yang sibuk - dianggap sangat berbahaya.
- Patologi berjangkit - khususnya jangkitan virus - juga boleh mewujudkan keadaan yang menggalakkan untuk perkembangan tumor. Adalah penting untuk mengingati perkara ini dan diberi vaksin terlebih dahulu, serta untuk mencegah penyakit berjangkit dan parasit.
- Keracunan tembakau dan alkohol dianggap sebagai faktor risiko untuk pelbagai jenis kanser, bukan hanya glioma otak.
- Aktiviti fizikal yang tidak mencukupi, berat badan berlebihan, pemakanan yang tidak betul, gangguan metabolik, kecederaan kepala, patologi vaskular - faktor tekanan tambahan yang boleh mencetuskan permulaan gangguan intraselular.
- Umur yang lebih tua adalah tempoh yang paling biasa untuk perkembangan neoplasma dalam badan, jadi mereka yang berumur lebih dari 55 tahun harus menjaga kesihatan mereka sendiri.
Walau bagaimanapun, faktor risiko utama dan paling ketara untuk perkembangan glioma kekal sebagai kecenderungan keturunan.
Patogenesis
Sehingga kini, pakar mempunyai beberapa andaian mengenai perkembangan glioma otak. Setiap teori mempunyai asasnya sendiri, tetapi satu-satunya mekanisme patogenetik yang betul dan boleh dipercayai saintis belum mengenal pasti. Dalam kebanyakan kes, kita bercakap tentang faktor berikut dalam perkembangan neoplasma:
Kegagalan embriogenesis, yang terdiri daripada gangguan peletakan organ dan pembentukan struktur sel "salah";
- Pendedahan kepada sinaran mengion, potensi karsinogen dalam bentuk agen kimia, bahan tambahan makanan, dsb.;
- Trauma kepala;
- Gangguan gen yang diwarisi dari generasi ke generasi (glioma "keluarga");
- Disfungsi imun, jangkitan saraf.
Kebanyakan glioma mempunyai pertumbuhan meresap, dengan penembusan ke dalam tisu otak normal di sekelilingnya. Bergantung pada tahap keganasan, tumor boleh berkembang selama beberapa tahun tanpa sebarang manifestasi. Dalam kes kursus yang agresif, simptomologi meningkat dengan cepat selama beberapa bulan.
Sebahagian daripada tumorigenesis adalah disebabkan oleh perubahan disembriogenetik.
Batang otak boleh terjejas pada tahap yang berbeza: glioma batang otak meresap, seterusnya, akan berbeza secara anatomi-morfologi dan klinikal. Sesetengah neoplasma sedemikian - khususnya, glioma plat quadriplegia - boleh menjadi agak jinak, tanpa tanda-tanda perkembangan. Sebaliknya, glioma pontine dicirikan oleh keganasan, keagresifan, dan prognosis yang buruk.
Lesi meresap struktur otak, di mana lebih daripada tiga zon anatomi hemisfera besar terlibat dalam proses patologi, dengan kemungkinan divergensi periventrikular dan laluan melalui gliomatosis panggilan korpus. [ 4 ]
Adakah glioma otak adalah keturunan?
Risiko pembentukan glioma otak yang terbukti dengan baik adalah keturunan - iaitu, kehadiran tumor intracerebral yang serupa atau lain dalam nenek moyang langsung atau dalam generasi yang sama. Pendedahan radioaktif dan sentuhan tetap atau berpanjangan dengan potensi karsinogen memburukkan lagi keadaan.
Bukan sahaja glioma boleh diwarisi, tetapi juga penyakit yang disertai dengan pertumbuhan tumor yang meningkat tanpa merujuk kepada penyetempatan - khususnya, ini mungkin neurofibromatosis jenis 1 dan 2, sindrom Li-Fraumeni, Hippel-Lindau. Selalunya dalam sel glioma, perubahan dalam gen atau kromosom tertentu dikesan.
Patologi utama yang dikaitkan dengan perkembangan glioma pada manusia diringkaskan dalam jadual:
Patologi |
Kromosom |
Gen |
Pelbagai neoplasma |
Sindrom Li-Fraumeni |
17р13 |
TR53 |
Neoplasma neuroectodermal, astrocytoma. |
Neurofibromatosis |
17q11 |
NF1 |
Glioma saraf optik, astrocytoma pilocytic, neurofibromatosis |
Sindrom Turcotte |
3p21, 7p22 |
HMLH1, HPSM2 |
Astrocytoma |
Sklerosis ubi (sindrom Burneville). |
9q34, 16p13 |
TSC1, TSC2 |
Astrocytoma subependymal gigantoselular |
Terlepas dari sifat tumor glial, sama ada ia adalah kes sporadis atau patologi keturunan, ia adalah gangguan dengan ekspresi gen yang diubah secara patologi. Selain daripada neoplasma yang terbentuk akibat daripada kesan pembelajaran, dalam situasi lain punca perubahan genetik masih tidak jelas.
Gejala daripada glioma otak
Ciri-ciri simptomologi fokus secara langsung bergantung pada kawasan penyetempatan glioma otak dan menjadi akibat daripada semua jenis gangguan endokrin, mampatan tisu saraf atau proses pemusnahan tempatan.
Sekiranya neoplasma terletak di zon parietal, maka seseorang dikuasai oleh manifestasi seperti sawan, gangguan deria, gangguan pendengaran.
Apabila glioma disetempat di kawasan hemisfera yang dominan, gangguan pertuturan, agraphia, agnosia dikesan.
Neoplasma lobus temporal sering disertai dengan sawan konvulsi, afasia, deria bau dan fungsi penglihatan terjejas, dan dyspnea.
Apabila tekanan intrakranial meningkat, gambaran yang sepadan berkembang dengan sekatan medan penglihatan, kelumpuhan otot mata, dan hemiplegia.
Oleh kerana kekhususan proses tumor, glioma otak sentiasa disertai oleh gejala neurologi ke tahap yang lebih besar atau lebih kecil. Pada mulanya, terdapat kelemahan umum yang ketara, pesakit sentiasa mahu tidur, keupayaan untuk bekerja terjejas, proses pemikiran menjadi perlahan. Pada peringkat ini terdapat risiko tinggi untuk membuat diagnosis yang salah dan, sebagai akibatnya, menetapkan rawatan yang salah. Antara manifestasi tidak spesifik lain:
- Gangguan vestibular, termasuk berjalan tidak stabil, kehilangan keseimbangan (cth, semasa berbasikal atau menaiki tangga), kebas pada anggota badan, dsb;
- Kemerosotan penglihatan secara beransur-ansur, menggandakan gambar visual;
- Kemerosotan fungsi pendengaran;
- Pertuturan yang tidak jelas;
- Mual dan muntah dalam bentuk serangan bebas daripada makanan atau minuman;
- Kelemahan otot mimik dan otot muka lain;
- Ketidakselesaan apabila menelan;
- Sakit kepala yang kerap (selalunya pada waktu pagi).
Gambar klinikal secara beransur-ansur berkembang dan bertambah buruk: pada sesetengah pesakit ia berlaku perlahan-lahan, pada yang lain - secara tiba-tiba, secara literal "di hadapan mata mereka", dalam masa beberapa minggu. Dalam kes kedua, kita bercakap tentang glioma otak yang agresif dan berkembang pesat.
Tanda-tanda pertama
Glioma otak pada peringkat awal perkembangan tidak mempunyai simptomologi yang jelas. Manifestasi pertama sering disalah anggap sebagai tanda-tanda patologi lain yang kurang berbahaya.
Secara umum, gambaran klinikal glioma adalah pelbagai dan ditentukan oleh lokasi dan saiz fokus patologi. Apabila neoplasma berkembang, gejala serebrum umum berkembang dan meningkat:
- Sakit kepala yang berterusan dan tetap yang tidak bertindak balas terhadap ubat standard (ubat anti-radang bukan steroid);
- Loya sekejap-sekejap, kadang-kadang sehingga muntah;
- Rasa tidak selesa dan berat di kawasan bola mata;
- sawan.
Manifestasi serebrum amat sengit apabila tumor tumbuh ke dalam ventrikel atau sistem minuman keras. Saliran cecair serebrospinal terjejas, tekanan intrakranial meningkat, dan hidrosefalus berkembang. Proses ini menjejaskan bahagian otak tertentu, yang mempengaruhi perkembangan klinik yang sepadan:
- Terdapat masalah dengan fungsi visual;
- Cacat pertuturan;
- Gangguan vestibular (pening, gangguan koordinasi pergerakan) berlaku;
- Paresis, lumpuh lengan, kaki;
- Ingatan dan tumpuan terjejas;
- Proses pemikiran terjejas;
- Gangguan tingkah laku muncul.
Pada peringkat awal, gejala hampir tidak hadir, atau mereka sangat tidak penting sehingga tidak menarik perhatian. Atas sebab inilah pakar sangat menasihati pemeriksaan dan pemeriksaan pencegahan secara berkala. Lagipun, lebih awal proses tumor dikesan, lebih besar peluang untuk sembuh dan terus hidup. [ 5 ]
Glioma otak pada kanak-kanak
Di antara banyak tumor otak yang ditemui pada zaman kanak-kanak, peratusan glioma berkisar antara 15 hingga 25%. Kanak-kanak boleh mendapat penyakit ini pada awal remaja dan awal dua puluhan, walaupun sangat jarang untuk bayi di bawah umur 3 tahun mendapat penyakit ini.
Patologi bermula dengan latar belakang mutasi sel glial. Sehingga kini, tiada jawapan kepada persoalan mengapa mutasi ini berlaku.
Satu-satunya perkara yang telah dipelajari dengan pasti ialah penyakit warisan tertentu yang dikaitkan dengan peningkatan risiko pertumbuhan tumor meningkatkan kemungkinan mengembangkan glioma otak juga.
Di samping itu, saintis telah mendapati bahawa sel glial boleh mempunyai perbezaan dalam gen atau kromosom individu. Kerana gangguan ini, mekanisme mutasi bermula, yang bukan keturunan. Kemungkinan ini berlaku pada salah satu peringkat perkembangan terawal.
Ia adalah fakta yang terbukti bahawa kehadiran leukemia akut atau retinoblastoma dalam sejarah kanak-kanak, atau penyinaran otak untuk sebarang sebab lain, meningkatkan risiko pembentukan glioma dengan ketara (selepas tempoh masa tertentu).
Symptomatology pada zaman kanak-kanak bergantung pada tahap keganasan dan penyetempatan fokus patologi. Perbezaan dibuat antara gejala khusus dan tidak spesifik:
- Gejala tidak spesifik tidak "terikat" pada kawasan di mana glioma berada. Manifestasi biasa mungkin termasuk sakit kepala, pening, kurang selera makan, muntah tanpa kaitan dengan pengambilan makanan, penurunan berat badan (atas sebab yang tidak diketahui), rasa keletihan yang berterusan, penurunan prestasi akademik, kesukaran dalam penumpuan, gangguan tingkah laku. Tanda-tanda ini disebabkan oleh pemampatan struktur intrakranial, yang boleh dijelaskan sebagai tekanan langsung jisim yang semakin meningkat, dan gangguan dalam peredaran cecair serebrospinal. Terdapat risiko hidrokel serebrum.
- Simptomologi khusus bergantung pada lokasi segera fokus patologi glial. Sebagai contoh, tumor cerebellar biasanya disertai dengan gangguan berjalan dan keseimbangan pada kanak-kanak. Lesi otak besar ditunjukkan oleh sawan sawan, dan pertumbuhan tumor dalam saraf tunjang - lumpuh otot. Ia berlaku bahawa penglihatan bayi merosot secara mendadak, kesedaran terganggu, tidur terganggu, atau beberapa masalah perkembangan lain berlaku.
Sebagai peraturan, pada zaman kanak-kanak, glioma malignan mendedahkan dirinya dalam beberapa minggu atau bulan perkembangannya: sering dicirikan oleh pertumbuhan pesat dan tidak terkawal neoplasma.
Kanak-kanak dengan tumor glial malignan dirawat oleh doktor di pusat klinikal pediatrik yang pakar dalam onkologi pediatrik. Sebagai peraturan, rawatan pembedahan, sinaran dan kursus kemoterapi digunakan.
Langkah rawatan yang paling penting ialah pembedahan saraf. Lebih radikal, lebih baik peluang kanak-kanak untuk sembuh. Tetapi campur tangan pembedahan tidak selalu mungkin: khususnya, masalah mungkin timbul dengan penyingkiran glioma batang otak, serta dengan radiasi untuk kanak-kanak di bawah umur 3 tahun.
Glioma otak tengah (perantaraan dan otak tengah) sukar untuk dikeluarkan sepenuhnya, kerana terdapat risiko kerosakan pada tisu yang sihat. Sekiranya reseksi lengkap tumor adalah mustahil, pesakit ditetapkan rawatan paliatif.
Kanak-kanak dengan glioma malignan dirawat mengikut protokol piawai yang telah ditentukan melalui ujian klinikal yang dikawal ketat. Protokol yang paling biasa adalah seperti berikut:
- HIT HGG 2007: melibatkan rawatan kanak-kanak berumur 3-17 tahun.
- HIT SKK: sesuai untuk bayi (sehingga tiga tahun) dan tidak melibatkan rawatan sinaran.
Statistik survival kanak-kanak untuk glioma biasanya tidak begitu optimistik. Walau bagaimanapun, dalam keadaan tidak mungkin untuk meramalkan terlebih dahulu keberkesanan langkah rawatan untuk kanak-kanak tertentu. Adalah penting untuk mematuhi semua arahan doktor dengan teliti, yang dengan ketara meningkatkan peluang pemulihan.
Borang
Glioma boleh menjadi malignan rendah dan malignan tinggi, dengan pertumbuhan yang sengit dan kecenderungan untuk bermetastasis. Adalah penting untuk memahami bahawa keganasan rendah tidak sinonim dengan keselamatan tumor. Mana-mana neoplasma otak mencipta jumlah tambahan, memerah struktur otak, yang membawa kepada anjakan mereka dan peningkatan tekanan intrakranial. Akibatnya, pesakit mungkin mati.
Terdapat dua jenis utama astrocytoma malignan. Ini adalah glioblastoma dan astrocytoma anaplastik, yang dibahagikan mengikut perubahan molekul. Tumor malignan sekunder yang berkembang daripada astrocytomas dan mempunyai tahap keganasan yang rendah paling kerap dijumpai pada pesakit muda. Pada mulanya tumor jenis glial malignan berlaku lebih kerap pada pesakit tua.
Bergantung pada lokasi struktur, glioma masuk:
- Supratentorial (dengan penyetempatan di atas cerebellum di kawasan ventrikel sisi, hemisfera besar);
- Subtentorial (dengan penyetempatan di bawah cerebellum dalam fossa kranial posterior).
Menurut ciri histologi, bezakan jenis glioma tersebut:
- Glioma astrocytic adalah yang paling biasa. Sebaliknya, ia dibahagikan kepada nodular dan meresap (yang terakhir boleh dicirikan oleh pertumbuhan pesat dan corak strok).
- Oligodendroglioma - berlaku dalam 5% pesakit. Ia mempunyai petrificates - kawasan kalsifikasi, paling kerap di lobus hadapan.
- Ependymal glioma - tumbuh dari struktur yang melapisi dinding saluran pusat saraf tunjang dan ventrikel. Selalunya tumbuh menjadi ketebalan bahan otak, serta ke dalam lumen otak.
Tumpuan patologi bercampur seperti subependymoma, oligoastrocytoma, dll. Juga mungkin.
Semua glioma dikategorikan ke dalam peringkat berikut:
- Neoplasma yang agak jinak yang tumbuh perlahan tanpa gejala klinikal yang jelas.
- Glioma "garis sempadan" tumbuh perlahan yang beransur-ansur berubah menjadi peringkat III dan seterusnya.
- Glioma malignan.
- Glioma malignan dengan pertumbuhan dan penyebaran agresif yang sengit, dengan prognosis yang buruk.
Semakin rendah tahap keganasan, semakin kecil kemungkinan metastasis dan berulangnya neoplasma yang dikeluarkan, dan semakin besar peluang untuk menyembuhkan pesakit. Bahaya terbesar ialah glioblastoma multiforme, proses yang dibezakan rendah dengan pertumbuhan dan perkembangan intensif. [ 6 ]
Varian neuroglioma yang mungkin dan paling biasa:
- Glioma dengan lesi batang otak dan pontine terletak di kawasan di mana otak bersambung ke saraf tunjang. Di sanalah pusat neuro penting yang bertanggungjawab untuk fungsi pernafasan, jantung, dan motor disetempatkan. Sekiranya zon ini rosak, kerja alat vestibular dan pertuturan terganggu. Ia sering dikesan pada zaman kanak-kanak.
- Glioma visual menjejaskan sel neuroglial yang mengelilingi saraf optik. Patologi menyebabkan kecacatan penglihatan dan exophthalmos. Ia berkembang lebih kerap pada kanak-kanak.
- Neuroglioma malignan rendah dicirikan oleh pertumbuhan perlahan, lebih kerap disetempat di hemisfera besar dan otak kecil. Ia lebih kerap berlaku pada orang muda (remaja dan dewasa muda sekitar 20 tahun).
- Glioma korpus callosum adalah lebih ciri individu yang berumur antara 40 dan 60 tahun dan paling biasa diwakili oleh glioblastoma.
- Glioma chiasma disetempat di zon persimpangan optik, jadi ia disertai dengan rabun, kehilangan medan penglihatan, hidrosefalus oklusif, dan gangguan neuroendokrin. Ia boleh berlaku pada mana-mana umur, tetapi paling kerap menjejaskan pesakit dengan neurofibromatosis jenis I.
Komplikasi dan akibatnya
Glioma keganasan rendah (Gred I-II, sangat malignan - cth, astrocytoma, oligoastrocytoma, oligodendroglioma, xanthoastrocytoma pleomorphic, dll.) dan keganasan tinggi (Gred III-IV - glioblastoma, oligodendroglioma anaplastik, oligoastrocytoma, dan astrocytoma). Glioma gred IV adalah terutamanya malignan.
Glioma batang otak mempunyai prognosis yang sangat tidak menguntungkan kerana neoplasma menjejaskan kawasan otak sedemikian, di mana sambungan saraf yang paling penting antara otak dan anggota badan tertumpu. Malah tumor yang agak kecil di kawasan ini sudah cukup untuk menjadikan keadaan pesakit cepat merosot dan mencetuskan lumpuh.
Tidak kurang akibat yang tidak menguntungkan berlaku apabila kawasan otak lain terjejas. Selalunya ia adalah tumor korteks serebrum, yang tidak memberi peluang untuk jangka hayat pesakit yang panjang, walaupun rawatan. Selalunya hanya mungkin untuk menangguhkan kematian.
Menurut statistik perubatan, kadar kelangsungan hidup lima tahun selalunya hanya 10-20%. Walaupun angka-angka ini sebahagian besarnya bergantung pada kedua-dua tahap keganasan dan penyetempatan yang tepat dan jumlah campur tangan pembedahan yang dilakukan. Selepas penyingkiran lengkap fokus patologi, kadar survival meningkat dengan ketara (kadang-kadang - sehingga 50%). Kekurangan rawatan atau kemustahilannya (untuk satu sebab atau yang lain) dijamin membawa kepada kematian pesakit.
Majoriti tumor glial malignan rendah mampu menyusup ke tisu otak dan memfitnah selama beberapa tahun.
Risiko berulang glioma dianggap oleh pakar sebagai "sangat berkemungkinan". Walau bagaimanapun, rawatan tidak boleh diabaikan: adalah penting untuk memastikan kualiti hidup yang baik selama mungkin.
Glioma berulang sentiasa mempunyai prognosis yang lebih buruk daripada tumor primer. Walau bagaimanapun, protokol rawatan moden berdasarkan kajian pengoptimuman terapeutik sering mencapai hasil yang cukup baik untuk pesakit walaupun dengan neoplasma yang sangat malignan.
Hasil yang mungkin selepas kemoterapi:
- Kurus, kurus, gangguan pencernaan, penyakit mulut;
- Peningkatan keceriaan sistem saraf pusat, asthenia;
- Kemerosotan fungsi pendengaran, tinnitus dan deringan di telinga;
- Kejang, gangguan kemurungan;
- Krisis hipertensi, perubahan dalam corak darah;
- Kegagalan buah pinggang;
- Proses alahan, keguguran rambut, penampilan bintik pigmen pada badan.
Selepas kemoterapi, pesakit mencatatkan kelemahan sistem imun yang ketara, yang boleh menyebabkan perkembangan pelbagai patologi berjangkit.
Diagnostik daripada glioma otak
Glioma otak boleh disyaki oleh tanda-tanda berikut:
- Pesakit mempunyai sawan setempat atau umum, yang merupakan ciri lokasi kortikal neoplasma dan perkembangannya yang perlahan. Epi-sawan ditemui dalam 80% pesakit dengan tumor glial gred rendah dan dalam 30% pesakit dengan glioma gred tinggi.
- Peningkatan tekanan intrakranial adalah ciri khas jisim yang terletak di lobus hadapan dan parietal kanan. Berkaitan dengan gangguan tekanan intrakranial yang tinggi dalam peredaran darah dan peredaran minuman keras melibatkan penampilan sakit kepala yang berterusan dan meningkat, loya dengan muntah, gangguan penglihatan, mengantuk. Terdapat edema saraf optik, lumpuh saraf pengalihan. Peningkatan tekanan intrakranial kepada nilai kritikal boleh membawa kepada perkembangan koma dan kematian. Satu lagi punca IOP tinggi ialah hidrosefalus.
- Pesakit mempunyai gambaran fokus yang semakin meningkat. Dalam pembentukan supratentorial, sfera motor dan deria terganggu, hemiopia, afasia, dan gangguan kognitif berkembang.
Sekiranya doktor mengesyaki kehadiran neoplasma otak, adalah optimum untuk melakukan MRI tanpa atau dengan pengenalan agen kontras (gadolinium) untuk mengetahui lokasi, saiz, dan ciri tambahannya. Jika pengimejan resonans magnetik tidak dapat dilakukan, tomografi yang dikira dilakukan, dan spektroskopi resonans magnetik digunakan sebagai kaedah pembezaan. Walaupun bermaklumat kaedah diagnostik ini, diagnosis akhir dibuat hanya selepas pengesahan histologi semasa reseksi fokus tumor.
Memandangkan kriteria di atas, adalah disyorkan untuk memulakan diagnosis dengan sejarah menyeluruh, penilaian status somato-neurologi dan status fungsi. Status neurologi dinilai bersama-sama dengan penentuan kemungkinan gangguan intelek dan mnestik.
Ujian makmal yang disyorkan:
- Pemeriksaan darah klinikal am sepenuhnya;
- Panel kimia darah penuh;
- Urinalisis;
- Kajian pembekuan darah;
- Analisis untuk penanda onkologi (AFP, beta-hCG, LDH - relevan jika lesi zon pineal disyaki).
Untuk menjelaskan titik prognostik pada pesakit dengan glioblastoma dan astrocytoma anaplastik, mutasi gen IDH1 | 2-1 dan metilasi gen MGMT dinilai. Pada pesakit dengan oligodendroglioma dan oligoastrocytoma, codlelation 1p|19q ditentukan.
Diagnostik instrumental, pertama sekali, diwakili oleh pengimejan resonans magnetik wajib otak (kadang-kadang - dan saraf tunjang). MRI dilakukan dalam tiga unjuran menggunakan mod T1-2, FLAIR, T1 standard dengan kontras.
Apabila ditunjukkan, ultrasound rangkaian vaskular, pengimejan resonans magnetik berfungsi bahagian motor dan pertuturan, serta angiografi, spektroskopi, MR tractography dan perfusi dilakukan.
Siasatan tambahan mungkin termasuk:
- Electroencephalography otak;
- Perundingan dengan pakar bedah saraf, pakar onkologi, pakar radiologi, pakar mata, pakar radiologi.
Diagnosis pembezaan
Diagnosis pembezaan semestinya dijalankan dengan patologi bukan tumor - khususnya, dengan pendarahan yang disebabkan oleh kecacatan arterio-vena atau arteri, serta dengan proses demielinasi pseudotumor, penyakit radang (toksoplasmosis, abses otak, dll.).
Di samping itu, bezakan fokus tumor utama dan metastasis sistem saraf pusat.
Dengan keupayaan pengimejan resonans magnetik moden, adalah mungkin untuk melakukan langkah diagnostik dengan cukup tepat, untuk mengetahui asal-usul fokus utama dalam CNS. MRI otak dilakukan dengan atau tanpa kontras, dalam mod T1, T2 FLAIR - dalam tiga unjuran, atau hirisan nipis dalam unjuran paksi (mod SPGR). Kaedah diagnostik ini membolehkan untuk menentukan dengan tepat lokasi, saiz, ciri-ciri struktur neoplasma, hubungannya dengan rangkaian vaskular dan kawasan otak yang berdekatan.
Selain itu, CT (dengan atau tanpa kontras), CT angiography (MR angiography), MR tractography, MR atau CT perfusi boleh dilakukan sebagai sebahagian daripada diagnosis pembezaan. CT/PET otak dengan metionin, kolin, tirosin, dan asid amino lain digunakan apabila ditunjukkan.
Rawatan daripada glioma otak
Terapi khusus terdiri daripada langkah-langkah pembedahan, kemoterapi dan sinaran. Ia adalah wajib, jika boleh, untuk melakukan reseksi lengkap fokus tumor, yang membolehkan pelepasan gejala cepat dan pengesahan histologi diagnosis.
Penyinaran mempunyai kesan positif untuk meningkatkan jangka hayat pesakit. Jumlah dos 58 hingga 60 Gy, dibahagikan kepada dos penyinaran individu 1.8-2 Gy, ditadbir sebagai standard. Tumor disinari secara tempatan, tambahan menangkap sehingga 3 cm di sekelilingnya. Terapi sinaran lebih boleh diterima berbanding dengan brachytherapy. Dalam sesetengah kes, kaedah radiosurgikal disyorkan, yang terdiri daripada penyinaran dengan Pisau Gamma atau pedal gas linear, serta terapi boron tangkapan neutron.
Keperluan untuk kemoterapi adjuvant adalah kontroversi. Dalam sesetengah kes, persediaan nitrosourea dibenarkan untuk meningkatkan jangka hayat pesakit sehingga satu setengah tahun, tetapi beberapa keputusan menggunakan kemopreparasi sedemikian adalah negatif. Hari ini, agen sitotoksik, terapi neoadjuvant (sebelum sinaran), ubat gabungan, kemoterapi intra-arteri, atau kemoterapi dos tinggi dengan pemindahan sel stem selanjutnya digunakan secara aktif.
Secara umum, untuk rawatan glioma yang berjaya, pendekatan komprehensif adalah sangat penting, sejauh mana bergantung pada lokasi dan tahap keganasan jisim, saiznya dan kesihatan umum pesakit.
Berhubung dengan glioma batang otak, campur tangan pembedahan jarang digunakan. Kontraindikasi utama untuk pembedahan adalah kawasan penyetempatan tumpuan - berdekatan dengan bahagian penting. Dalam sesetengah kes, adalah mungkin untuk mengeluarkan glioma batang menggunakan kaedah mikrosurgikal, dengan kemoterapi pra operasi dan selepas operasi. Intervensi sedemikian adalah sangat kompleks dan memerlukan kelayakan khas pakar bedah saraf.
Pembedahan sinaran dan, khususnya, pembedahan stereotaktik dengan pendedahan kepada dos pengionan yang tinggi adalah agak berkesan. Penggunaan teknik sedemikian pada peringkat awal perkembangan neoplasma kadang-kadang membolehkan untuk mencapai remisi yang berpanjangan atau bahkan penyembuhan lengkap pesakit.
Radiasi sering digabungkan dengan kemoterapi, yang meningkatkan keberkesanan intervensi dan mengurangkan beban radiasi. Dalam glioma, tidak semua agen kemopreventif berjaya secara terapeutik, jadi ia ditetapkan secara individu dan preskripsi diselaraskan jika perlu.
Untuk mengurangkan kesakitan dan tekanan intrakranial yang lebih rendah, tanpa mengira rawatan utama, terapi gejala ditetapkan - khususnya, ubat kortikosteroid, analgesik, sedatif.
Ubat-ubatan
Ubat kortikosteroid menjejaskan bengkak, mengurangkan keterukan gejala neurologi selama beberapa hari. Walau bagaimanapun, disebabkan oleh pelbagai kesan sampingan dan peningkatan kemungkinan interaksi buruk dengan ubat kemoterapi, dos steroid yang berkesan minimum digunakan, menghentikannya secepat mungkin (cth, selepas pembedahan).
Antikonvulsan digunakan secara sistematik sebagai langkah pencegahan sekunder pada pesakit yang telah mengalami sawan epilepsi. Ubat-ubatan ini boleh menyebabkan gejala buruk yang serius dan juga berinteraksi dengan ubat kemoterapi.
Antikoagulan amat relevan pada peringkat pasca operasi, kerana risiko pembentukan trombophlebitis dalam glioma agak tinggi (sehingga 25%).
Kesan yang baik dijangka daripada mengambil antidepresan-anxiolytics. Penggunaan Methylphenidate 10-30 mg/hari dalam dua dos selalunya membolehkan untuk mengoptimumkan kebolehan kognitif, meningkatkan kualiti hidup, mengekalkan kapasiti kerja.
Kegagalan neurologi dan tanda-tanda edema serebrum (sakit di kepala, gangguan kesedaran) dihapuskan oleh ubat kortikosteroid - khususnya, Prednisolone atau Dexamethasone. |
Skim dan dos kortikosteroid dipilih secara individu, dengan amalan dos berkesan minimum. Pada akhir kursus rawatan, ubat-ubatan secara beransur-ansur ditarik balik. |
Kortikosteroid diambil bersama dengan ubat gastroprotektif - penyekat pam proton atau Penyekat H2-histamin. |
Diuretik (Furosemide, Mannitol) ditetapkan untuk pembengkakan teruk dan anjakan struktur otak, sebagai tambahan kepada ubat kortikosteroid. |
Dalam kes sawan sawan (termasuk anamnesis) atau gejala epileptiform pada electroencephalogram, terapi antikonvulsan juga ditetapkan. Antikonvulsan tidak ditetapkan untuk tujuan profilaksis. |
Pesakit dengan tanda-tanda untuk kemoterapi disyorkan untuk mengambil antikonvulsan yang tidak menjejaskan fungsi enzim hati. Ubat pilihan: Lamotrigin, asid Valproik, Levetiracetam. Tidak boleh digunakan: Carbamazepine, Phenobarbital. |
Sakit kepala dalam glioma otak diuruskan dengan rawatan kortikosteroid. |
Dalam sesetengah kes sakit kepala, ubat anti-radang bukan steroid atau tramadol boleh digunakan. |
Jika pesakit mengambil ubat anti-radang bukan steroid, ia dihentikan beberapa hari sebelum pembedahan untuk meminimumkan kemungkinan pendarahan semasa pembedahan. |
Dalam kes kesakitan yang terpilih, analgesik narkotik - seperti Fentanyl atau Trimeperidine - mungkin disyorkan. |
Untuk mengelakkan embolisme pulmonari dari hari ketiga selepas operasi, pemberian heparin berat molekul rendah - khususnya, natrium Enoxaparin atau kalsium Nadroparin - ditetapkan. |
Sekiranya pesakit menjalani rawatan antikoagulan atau antiagregat yang sistematik, dia dipindahkan ke heparin berat molekul rendah selewat-lewatnya seminggu sebelum campur tangan pembedahan, dengan pengeluaran selanjutnya sehari sebelum pembedahan dan disambung semula 24-48 jam selepas pembedahan. |
Sekiranya pesakit dengan glioma mempunyai trombosis vena pada bahagian bawah kaki, rawatan dengan antikoagulan langsung dilakukan. Kemungkinan meletakkan penapis CAVA tidak dikecualikan. |
Kemoterapi untuk glioma malignan otak
Rejimen kemoterapi antitumor asas untuk glioma dianggap sebagai:
- Lomustine 100 mg/m² pada hari pertama, Vincristine 1.5 mg/m² pada hari pertama dan lapan, Procarbazine 70 mg/m² dari hari kelapan hingga dua puluh satu, kursus setiap enam minggu.
- Lomustine 110 mg/m² setiap enam minggu.
- Temozolomide 5/23 150 hingga 200 mg/m² dari hari pertama hingga hari kelima, setiap 28 hari.
- Temozolomide sebagai sebahagian daripada rawatan kemoradiasi, 75 mg/m² setiap hari yang sinaran diberikan.
- Temozolomide dengan Cisplatin atau Carboplatin (80 mg/m²), dan Temozolomide 150-200 mg/m² pada hari 1 hingga 5 setiap 4 minggu.
- Temozolomide 7/7 pada 100 mg/m² pada hari 1-8 dan 15-22 kursus, dengan ulangan setiap empat minggu.
- Bevacizumab 5 hingga 10 mg/kg pada hari satu dan lima belas, dan Irinotecan 200 mg/m² pada hari satu dan lima belas, diulang setiap empat minggu.
- Bevacizumab 5 hingga 10 mg/kg pada hari pertama, lima belas dan dua puluh sembilan, dan Lomustine 90 mg/m² pada hari pertama setiap enam minggu.
- Bevacizumab 5 hingga 10 mg/kg pada hari pertama dan lima belas, Lomustine 40 mg pada hari pertama, lapan, lima belas, dan dua puluh dua, diulang setiap enam minggu.
- Bevacizumab 5 hingga 10 mg/kg pada hari pertama dan lima belas, diulang setiap empat minggu.
Ubat sitostatik dalam banyak kes berjaya menghalang pertumbuhan sel tumor, tetapi tidak menunjukkan selektiviti terhadap tisu dan organ yang sihat. Oleh itu, pakar telah mengenal pasti beberapa kontraindikasi di mana kemoterapi glioma adalah mustahil:
- Kepekaan individu yang berlebihan kepada agen chemopreventive;
- Dekompensasi fungsi jantung, buah pinggang, hati;
- hematopoiesis tertekan dalam sumsum tulang;
- Masalah fungsi adrenal.
Kemoterapi diberikan dengan sangat berhati-hati:
- Pesakit dengan gangguan irama jantung yang ketara;
- Dengan diabetes;
- Untuk jangkitan virus akut;
- Kepada pesakit warga emas;
- Pesakit yang menghidap alkoholisme kronik (mabuk alkohol kronik).
Kesan sampingan ubat chemopreventive yang paling serius ialah ketoksikannya: sitostatik secara selektif mengganggu fungsi sel darah dan mengubah komposisinya. Akibatnya, jisim platelet dan eritrosit berkurangan dan anemia berkembang.
Sebelum menetapkan kursus kemoterapi kepada pesakit, doktor sentiasa mengambil kira tahap ketoksikan ubat-ubatan dan kemungkinan komplikasi selepas penggunaannya. Kursus kemoterapi sentiasa dipantau dengan teliti oleh pakar dan pemantauan darah secara berkala.
Kemungkinan akibat terapi sitostatik:
- Kurus, kurus;
- Kesukaran menelan makanan, membran mukus kering, periodontitis, dispepsia;
- Ketidakstabilan sistem saraf pusat, gangguan manik-depresi, sindrom sawan, asthenia;
- Kemerosotan fungsi pendengaran;
- Peningkatan tekanan darah sehingga perkembangan krisis hipertensi;
- Penurunan platelet, sel darah merah, sel darah putih, pendarahan berganda, pendarahan dalaman dan luaran;
- Kegagalan buah pinggang;
- Proses alahan;
- Keguguran rambut, penampilan kawasan pigmentasi meningkat.
Selepas kursus kemoterapi, pesakit mempunyai peningkatan risiko mendapat penyakit berjangkit, dan sakit otot dan sendi adalah perkara biasa.
Untuk mengurangkan risiko kesan buruk selepas kemoterapi, langkah-langkah pemulihan selanjutnya semestinya ditetapkan, tujuannya adalah untuk memulihkan kiraan darah normal, penstabilan aktiviti kardiovaskular, normalisasi status neurologi. Sokongan psikologi yang mencukupi semestinya diamalkan.
Rawatan pembedahan
Pembedahan dilakukan untuk membuang fokus tumor sebanyak mungkin, yang seterusnya akan mengurangkan tekanan intrakranial, mengurangkan ketidakcukupan neurologi, dan menyediakan biomaterial yang diperlukan untuk penyelidikan.
- Pembedahan dilakukan di jabatan atau klinik neurosurgi khusus yang pakarnya berpengalaman dalam campur tangan neuro-onkologi.
- Pakar bedah melakukan akses dengan trepanasi tulang plastik di kawasan penyetempatan glioma yang disyaki.
- Jika neoplasma terletak secara anatomi dekat dengan kawasan motor atau laluan, atau dalam nukleus atau sepanjang saraf kranial, pemantauan neurofisiologi intraoperatif digunakan.
- Sistem neuronavigasi, navigasi pendarfluor intraoperatif dengan asid 5-aminolevulenik adalah wajar untuk memaksimumkan penyingkiran neoplasma.
- Selepas campur tangan, CT atau MRI kawalan (dengan atau tanpa suntikan kontras) dilakukan pada hari 1-2.
Jika reseksi pembedahan glioma adalah mustahil atau pada mulanya diiktiraf sebagai tidak sesuai, atau jika limfoma sistem saraf pusat disyaki, biopsi (terbuka, stereotaktik, dengan pemantauan navigasi, dll.) dilakukan. |
Pesakit dengan gliomatosis serebrum disahkan oleh biopsi stereotaktik, kerana taktik terapeutik sebahagian besarnya bergantung pada gambaran histologi. |
Dalam situasi tertentu - pada pesakit tua, dalam kes gangguan neurologi yang teruk, dalam kes penyetempatan glioma dalam batang dan bahagian penting lain - rawatan dirancang berdasarkan gejala dan maklumat pengimejan selepas perundingan perubatan am. |
Pesakit dengan astrocytoma piloid serta bentuk nodular neoplasma batang otak dan proses exophytic disyorkan untuk menjalani reseksi atau biopsi terbuka. |
Pesakit dengan glioma pontine meresap dan neoplasma meresap lain pada batang dirawat dengan terapi radiasi dan ubat antitumor. Pengesahan tidak diperlukan dalam kes sedemikian. |
Pesakit dengan glioma plat quadriplegic menjalani resonans magnetik sistematik dan pemantauan klinikal selepas penyingkiran hidrokel serebrum. Jika neoplasma menunjukkan tanda-tanda pertumbuhan, ia dikeluarkan dengan penyinaran selanjutnya. |
Apabila reseksi separa atau biopsi glioma malignan gred rendah dilakukan, pesakit yang mempunyai dua atau lebih faktor risiko semestinya dirawat dengan radiasi dan/atau kemoterapi. |
Jumlah reseksi adalah wajib untuk pesakit dengan astrocytoma sel gergasi subependymal. |
Everolimus ditetapkan untuk astrocytoma sel gergasi subependymal meresap. |
Piloid astrocytoma perlu dikeluarkan dengan pengimejan resonans magnetik selepas campur tangan untuk menjelaskan kualiti reseksi radikal tisu tumor. |
Dalam glioblastoma, terapi selepas pembedahan perlu digabungkan (radiasi + kemoterapi) dengan pentadbiran Temozolomide. |
Dalam astrocytoma anaplastik selepas pembedahan, terapi radiasi dengan terapi ubat lanjut ditunjukkan. Lomustine, Temozolomide digunakan. |
Pesakit dengan oligodendroglioma anaplastik atau oligoastrocytoma menerima kedua-dua radiasi dan kemoterapi (monoterapi Temozolomide atau PCV) selepas pembedahan. |
Pesakit tua dengan glioma malignan tinggi yang meluas disinari dalam mod hypofractionated, atau monoterapi dengan Temozolomide dilakukan. |
Sekiranya glioma berulang, kemungkinan operasi semula dan taktik rawatan seterusnya dibincangkan oleh konsilium pakar. Rejimen optimum untuk berulang: operasi semula + kemoterapi sistemik + pendedahan radiasi berulang + langkah paliatif. Jika terdapat kawasan kecil setempat pertumbuhan tumor berulang, radiosurgeri boleh digunakan. |
Ubat pilihan untuk pertumbuhan glioma berulang ialah Temozolomide dan Bevacizumab. |
Berulangnya oligodendrogliomas yang sangat malignan dan astrocytomas anaplastik adalah petunjuk untuk rawatan Temozolomide. |
Xanthoastrocytoma pleomorphic dikeluarkan tanpa kemoterapi adjuvant mandatori. |
Salah satu keanehan glioma adalah kesukaran dalam rawatan dan penyingkirannya. Pakar bedah bertujuan untuk mengeluarkan tisu neoplasma selengkap mungkin, untuk mencapai pampasan keadaan. Ramai pesakit dapat meningkatkan kualiti hidup dan memanjangkannya, tetapi untuk tumor yang sangat malignan prognosisnya tetap tidak menguntungkan: terdapat kemungkinan peningkatan pertumbuhan semula fokus patologi.
Pemakanan untuk glioma otak
Diet untuk pesakit dengan tumor malignan - satu perkara penting, yang, malangnya, ramai orang tidak memberi banyak perhatian. Sementara itu, terima kasih kepada perubahan dalam diet, ia adalah mungkin untuk melambatkan perkembangan glioma dan menguatkan dan goncang imuniti.
Bidang utama perubahan diet:
- Normalisasi proses metabolik, menguatkan perlindungan imun;
- Detoksifikasi badan;
- Pengoptimuman potensi tenaga;
- Memastikan fungsi normal semua organ dan sistem badan semasa tempoh yang sukar bagi mereka.
Pemakanan yang rasional dan seimbang adalah perlu, kerana pesakit dengan peringkat awal neoplasma malignan rendah, dan pesakit dengan peringkat terakhir glioblastoma. Diet yang dipilih dengan teliti menyumbang kepada peningkatan kesejahteraan umum, pemulihan tisu yang rosak, yang sangat penting terhadap latar belakang rawatan sitostatik dan radiasi. Keseimbangan komponen pemakanan dan proses metabolik yang betul menghalang pembentukan fokus berjangkit, menghalang tindak balas keradangan, mencegah keletihan badan.
Makanan dan minuman berikut disyorkan untuk glioma otak:
- Buah-buahan dan sayur-sayuran berwarna merah, kuning dan oren (tomato, pic, aprikot, lobak merah, bit, buah sitrus) yang mengandungi karotenoid, yang melindungi sel yang sihat daripada kesan negatif terapi sinaran;
- Kubis (kembang kol, brokoli, pucuk Brussels), lobak, mustard, dan produk tumbuhan lain yang mengandungi indole - bahan aktif yang meneutralkan faktor toksik dan kimia yang buruk;
- Hijau (dill, pasli, dandelion muda dan daun jelatang, rhubarb, arugula, bayam), kacang hijau dan asparagus, kacang asparagus, dan alga (rumpai laut, spirulina, chlorella);
- Teh hijau;
- Bawang putih, bawang merah, nanas, yang mempunyai keupayaan anti-tumor dan detoksifikasi;
- Dedak, bijirin, roti bijirin penuh, pucuk pucuk kekacang, bijirin dan biji;
- Anggur gelap, raspberi, strawberi dan strawberi, beri biru, beri hitam, delima, kismis, kismis hitam, rowanberi, beri biru, buckthorn laut, ceri dan beri lain yang mengandungi antioksidan semula jadi yang mengurangkan kesan negatif radikal bebas, virus dan karsinogen;
- Produk tenusu rendah lemak.
Anda tidak boleh membebankan sistem pencernaan dan seluruh badan dengan makanan berat dan berlemak. Ia berguna untuk menggunakan jus buatan sendiri yang baru diperah, smoothie, potongan. Sumber asid lemak omega-3, seperti minyak ikan, minyak biji rami atau biji rami, harus ditambah pada hidangan.
Adalah lebih baik untuk mengelakkan gula dan gula-gula sama sekali. Tetapi satu sudu madu dengan secawan air tidak akan menyakitkan: produk lebah mempunyai kesan anti-radang, antioksidan dan antitumor yang ketara. Satu-satunya kontraindikasi terhadap penggunaan madu adalah alahan kepada produk.
Daripada diet harus dikecualikan:
- Daging, lemak babi, jeroan;
- Mentega, produk tenusu berlemak;
- Daging asap, sosej, daging dalam tin dan ikan;
- Alkohol dalam sebarang bentuk;
- Gula-gula, pastri, kek dan pastri, gula-gula dan coklat;
- Makanan mudah, makanan segera, makanan ringan;
- Makanan bergoreng.
Anda perlu mengambil sayur-sayuran, sayur-sayuran, buah-buahan, dan air minuman bersih yang mencukupi setiap hari.
Semasa kemoterapi dan beberapa lama selepas itu, anda harus minum jus sayur-sayuran dan buah-buahan buatan sendiri, makan keju kotej rendah lemak buatan sendiri, susu dan keju. Adalah penting untuk minum banyak cecair, gosok gigi dan bilas mulut anda dengan kerap (kira-kira 4 kali sehari).
Makanan optimum untuk pesakit glioma otak:
- Kaserol sayur-sayuran;
- Hidangan sampingan dan sup yang diperbuat daripada bijirin (sebaik-baiknya soba, oat, nasi, couscous, bulgur);
- Kek keju kukus, puding, kaserol;
- Sayuran rebus dan bakar;
- Stews, sup sayur-sayuran, hidangan pertama dan kedua daripada kekacang (termasuk soya), paté dan soufflé;
- Smoothie, teh hijau, kolak dan potongan.
Pencegahan
Sekiranya seseorang menjalani gaya hidup yang sihat, dan di kalangan saudara-maranya tidak ada kes patologi kanser, dia mempunyai peluang untuk tidak mendapat glioma otak. Tiada pencegahan khusus untuk tumor sedemikian, jadi perkara pencegahan utama dianggap sebagai pemakanan yang betul, aktiviti fizikal, mengelakkan tabiat buruk, ketiadaan bahaya pekerjaan dan rumah tangga.
Pakar memberikan beberapa cadangan yang mudah tetapi berkesan:
- Minum lebih banyak air tulen, elakkan soda manis, jus yang dibungkus, minuman tenaga dan alkohol.
- Elakkan bahaya pekerjaan dan rumah: kurangkan sentuhan dengan bahan kimia, larutan yang menghakis dan cecair.
- Cuba sediakan makanan dengan merebus, merebus, membakar, tetapi tidak menggoreng. Beri keutamaan kepada makanan buatan sendiri yang sihat dan berkualiti.
- Sebilangan besar diet anda haruslah makanan tumbuhan, termasuk sayur-sayuran, tanpa mengira masa dalam setahun.
- Satu lagi faktor negatif ialah berat badan berlebihan, yang harus disingkirkan. Kawalan berat badan sangat penting untuk kesihatan seluruh badan.
- Minyak sayuran hendaklah sentiasa diutamakan berbanding mentega dan lemak babi.
- Jika boleh, adalah wajar untuk memberi keutamaan kepada produk mesra alam, daging tanpa hormon, sayur-sayuran dan buah-buahan tanpa nitrat dan racun perosak. Adalah lebih baik untuk mengelakkan daging merah sama sekali.
- Jangan mengambil persediaan multivitamin tanpa petunjuk dan dalam kuantiti yang banyak. Jangan ambil sebarang ubat tanpa preskripsi doktor: ubat sendiri selalunya sangat, sangat berbahaya.
- Sekiranya gejala yang mencurigakan muncul, adalah perlu untuk melawat doktor, tanpa menunggu keterukan keadaan, perkembangan kesan buruk dan komplikasi.
- Gula-gula dan makanan dengan indeks glisemik tinggi adalah komponen diet yang tidak diingini.
- Lebih awal seseorang pergi ke doktor, lebih baik peluangnya untuk sembuh (dan ini terpakai kepada hampir semua penyakit, termasuk glioma otak).
Untuk mengelakkan pembentukan onkopatologi, anda memerlukan masa yang cukup untuk tidur dan berehat, mengelakkan penggunaan minuman beralkohol yang berlebihan, memberi keutamaan kepada makanan semulajadi yang berkualiti tinggi, mengurangkan penggunaan alat (khususnya, telefon bimbit).
Penyakit tumor sering berlaku pada orang tua dan orang tua. Oleh itu, adalah penting untuk memantau kesihatan anda sendiri dari usia muda dan tidak mencetuskan proses patologi oleh gaya hidup yang tidak sihat dan tabiat yang tidak sihat.
Punca sebenar onkologi masih belum dijelaskan. Walau bagaimanapun, peranan tertentu, sudah tentu, memainkan keadaan pekerjaan dan alam sekitar yang tidak menguntungkan, pendedahan kepada sinaran pengion dan elektromagnet, perubahan hormon. Jangan tinggal lama dan kerap di bawah matahari, benarkan perubahan mendadak dalam suhu persekitaran, terlalu panas dalam bilik mandi atau sauna, kerap mandi air panas atau mandi.
Soalan lain: bagaimana untuk mencegah berulangnya glioma otak selepas rawatannya yang berjaya? Pertumbuhan neoplasma berulang adalah kompleks dan, malangnya, komplikasi yang kerap, yang sukar untuk diramalkan terlebih dahulu. Pesakit boleh disyorkan untuk menjalani pemeriksaan dan pemeriksaan pencegahan secara berkala, melawat pakar onkologi dan doktor yang merawat sekurang-kurangnya dua kali setahun, menjalani gaya hidup sihat, makan makanan yang sihat dan semula jadi, mengamalkan aktiviti fizikal sederhana. Syarat lain ialah cinta hidup, keyakinan yang sihat, sikap positif untuk berjaya dalam apa jua keadaan. Ini juga termasuk suasana mesra dalam keluarga dan di tempat kerja, kesabaran dan sokongan tanpa syarat daripada orang rapat.
Ramalan
Keadaan otak dan ciri-ciri glioma pada masa pengesanannya mempengaruhi kadar kelangsungan hidup sama seperti rawatan yang diberikan. Kesihatan umum pesakit dan umurnya yang memuaskan meningkatkan prognosis (prognosis lebih optimistik pada pesakit muda). Penunjuk penting ialah gambaran histologi neoplasma. Oleh itu, glioma gred rendah mempunyai prognosis yang lebih baik daripada glioma anaplastik dan, lebih-lebih lagi, glioblastoma (proses tumor yang paling tidak menguntungkan). Astrocytomas mempunyai prognosis yang lebih buruk daripada oligodendrogliomas.
Astrocytoma malignan bertindak balas dengan lemah terhadap terapi dan mempunyai kadar kelangsungan hidup yang agak rendah antara enam hingga lima tahun. Pada masa yang sama, jangka hayat dalam glioma gred rendah dianggarkan pada 1-10 tahun.
Astrocytoma malignan pada dasarnya tidak boleh diubati. Arah rawatan biasanya melibatkan pengurangan manifestasi neurologi (termasuk disfungsi kognitif) dan meningkatkan jangka hayat sambil mengekalkan kualiti hidup yang setinggi mungkin. Terapi simtomatik tertarik dengan latar belakang langkah-langkah pemulihan. Kerja ahli psikologi juga penting.
Sepanjang dekad yang lalu, saintis telah membuat sedikit kemajuan dalam memahami sifat tumor otak dan cara merawatnya. Banyak lagi yang perlu dilakukan untuk mengoptimumkan prognosis penyakit ini. Tugas utama pakar hari ini adalah yang berikut: glioma otak harus mempunyai beberapa skim untuk penghapusan masalah yang berkesan sekaligus, baik pada peringkat awal dan seterusnya perkembangan.

