Pakar perubatan artikel itu
Penerbitan baru
Peranan perubahan dalam tulang subkondral dalam patogenesis osteoarthritis
Ulasan terakhir: 04.07.2025

Semua kandungan iLive disemak secara perubatan atau fakta diperiksa untuk memastikan ketepatan faktual sebanyak mungkin.
Kami mempunyai garis panduan sumber yang ketat dan hanya memautkan ke tapak media yang bereputasi, institusi penyelidikan akademik dan, apabila mungkin, dikaji semula kajian secara medis. Perhatikan bahawa nombor dalam kurungan ([1], [2], dan lain-lain) boleh diklik pautan ke kajian ini.
Jika anda merasakan bahawa mana-mana kandungan kami tidak tepat, ketinggalan zaman, atau tidak dipersoalkan, sila pilih dan tekan Ctrl + Enter.
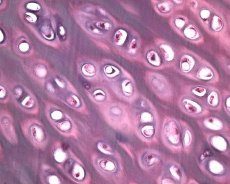
Bersama dengan degenerasi rawan artikular, tisu tulang yang mendasari juga terlibat dalam proses patologi dalam osteoarthrosis. Diandaikan bahawa penebalan plat subkondral menyumbang kepada perkembangan osteoarthrosis. Apabila osteoarthrosis berkembang, rawan artikular, yang tertakluk kepada tekanan mekanikal dan kimia, perlahan-lahan terhakis disebabkan oleh ketidakseimbangan dalam proses katabolisme dan pembaikan rawan. Khususnya, tekanan mekanikal berhubung dengan sendi "menanggung" berat badan menyumbang kepada pembentukan sejumlah besar patah mikro dalam plat subkondral dan tulang rawan. Apabila rawan artikular terhakis, sklerosis tulang subkondral berkembang, ketegaran tisu tulang meningkat, yang seterusnya menyumbang kepada gangguan lagi struktur rawan artikular. Walau bagaimanapun, persoalan sifat primer atau sekunder perubahan tulang subkondral dalam osteoarthrosis masih tidak dapat diselesaikan.
Sehingga baru-baru ini, perubahan yang dapat dikesan secara radiografi dalam bahan span tulang subkondral, seperti sklerosis atau pembentukan sista, dianggap sekunder pada pesakit dengan osteoarthrosis. Walau bagaimanapun, hasil kajian klinikal dan eksperimen menunjukkan kemungkinan peranan permulaan tulang subkondral dalam patogenesis osteoarthrosis. Salah satu mekanisme yang mungkin adalah peningkatan mendadak dalam kecerunan kekakuan tulang subkondral disebabkan oleh fakta bahawa integriti tisu tulang rawan yang mendasari bergantung pada sifat mekanikal "katil" tulangnya. Kajian pada primata telah menunjukkan bahawa perubahan dalam tulang subkondral boleh mendahului perubahan dalam rawan artikular. Bukti menyokong dan menentang hipotesis ini yang telah muncul sebagai hasil kajian dalam model haiwan osteoarthrosis dan kajian klinikal hanya memperhebatkan perdebatan. Penebalan trabekula dalam tulang subkondral tidak selalu disertai dengan peningkatan mineralisasi tulang, atau sebaliknya, peningkatan dalam jumlah osteoid. Tanda mineralisasi yang tidak normal ini menunjukkan bahawa gangguan peraturan pembentukan semula tulang adalah sebahagian daripada osteoarthritis dan juga menyokong konsep kecacatan sel tulang dalam osteoarthritis. Kumpulan J. Dequeker (1989) menganggap yang terakhir sebagai "penyakit tulang metabolik umum".
Tisu tulang sentiasa diperbaharui. Proses dinamik ini, yang dipanggil pembentukan semula tulang, adalah urutan resorpsi dan mineralisasi yang kompleks. Osteoklas menyerap tisu tulang, dan osteoblas merembeskan protein yang membentuk komponen organik utama untuk mineralisasi. Pembentukan dan penyerapan tulang tidak berlaku secara rawak di seluruh rangka; ia adalah proses terprogram yang berlaku di kawasan rangka yang berbeza, yang dipanggil unit pembentukan semula tulang. Pada awal kitaran, osteoklas muncul pada permukaan yang tidak aktif; dalam masa 2 minggu, mereka membentuk terowong dalam tulang kortikal atau lakuna pada permukaan tulang trabekular. Kekerapan pengaktifan unit pembentukan semula tulang baru menentukan tahap pembaharuan tulang. Dalam orang muda yang sihat, proses pembentukan dan penyerapan tulang adalah seimbang, dan jisim tulang normal dikekalkan. Dalam peraturan hormon penyerapan tisu tulang, sekurang-kurangnya PTH dan PGE2 , bukan sahaja osteoklas tetapi juga osteoblas mengambil bahagian, kerana di bawah pengaruh hormon ini, faktor-faktor yang merangsang penyerapan tulang oleh osteoklas dikeluarkan. Pada masa ini, lebih daripada 12 pengawal selia tempatan dan sistemik pertumbuhan tisu tulang diketahui yang mempengaruhi pembentukan semulanya, khususnya PTH, 1,25(OH) 2D3 ,kalsitonin, hormon pertumbuhan, glukokortikoid, hormon tiroid, insulin, IGF (1 dan 2), estrogen, PGE2 , androgen.
Sel-sel tulang membebaskan sejumlah protein dan sitokin yang melakukan pengawalan endokrin dan transduksi isyarat. Protein yang dihasilkan oleh osteoblas termasuk protein matriks tulang seperti kolagen, osteopontin, osteocalcin, sialoprotein tulang. Di samping itu, sel-sel ini membebaskan protease dalam kedua-dua bentuk aktif dan terpendam yang mengambil bahagian dalam proses pembentukan semula tisu tulang - MMP, komponen sistem pengaktif plasminogen (PA)/plasmin. Sitokin yang dikeluarkan oleh osteoblas boleh bertindak melalui mekanisme autokrin dan laluan parakrin pada sel tempatan (osteoblas lain, osteoklas).
Ia belum diketahui sama ada isyarat ini dikawal oleh tekanan mekanikal atau isyarat kimia lain yang disebabkan oleh tekanan mekanikal. Walau bagaimanapun, diketahui bahawa tekanan mekanikal yang berulang menyebabkan percambahan sel tulang dan/atau protein setempat. Dalam vivo, beban mekanikal boleh mengaktifkan osteoblas, meningkatkan tahap nukleotida kitaran, pengeluaran prostaglandin, dan menyebabkan perubahan morfologi yang berkaitan dengan pembentukan semula tulang. In vitro, tekanan mekanikal menyebabkan percambahan kultur osteoblas, ekspresi mRNA protein tulang yang terlibat dalam pembentukan dan mineralisasi osteoid, pembebasan faktor pertumbuhan tempatan seperti IGF-1 dan IGF-2, dan molekul lekatan. Penghantaran isyarat tegasan mekanikal boleh dilakukan melalui saluran ion mekanosensitif.
Terdapat bukti tidak langsung tentang disfungsi osteoblas dalam osteoarthrosis. G. Gevers dan J. Dequeker (1987) menunjukkan peningkatan paras osteocalcin serum pada wanita dengan osteoarthrosis tangan, serta dalam eksplan tulang kortikal, menunjukkan bahawa patologi tulang mungkin sebahagian daripada osteoarthrosis. Bedah siasat mendedahkan bukan sahaja penebalan tulang subkondral, tetapi juga mineralisasi rendah yang luar biasa pada kepala femoral. Dalam babi guinea dengan osteoarthrosis akibat pembedahan, tomografi yang dikira menunjukkan penebalan ketara pecahan tulang di zon subkondral. Ketidakseimbangan antara protein kolagen dan bukan kolagen (osteocalcin, dll.) boleh menyebabkan peningkatan dalam jumlah tulang, tetapi tidak menjejaskan ketumpatan mineralnya. Menurut M. Shimizu et al. (1993), perkembangan perubahan degeneratif dalam rawan artikular dikaitkan dengan pembentukan semula tulang subkondral yang lebih intensif dan peningkatan ketegarannya, yang juga menunjukkan kecacatan pada sel tisu tulang dalam osteoarthrosis. Menurut hipotesis yang dicadangkan oleh B. Lee dan M. Aspden (1997), percambahan sel tulang yang rosak boleh menyebabkan peningkatan ketegaran tisu tulang, tetapi tidak menyebabkan peningkatan ketumpatan mineralnya.
CI Westacott et al. (1997) membuat hipotesis bahawa osteoblas yang tidak normal secara langsung mempengaruhi metabolisme rawan. Menanam osteoblas daripada pesakit dengan osteoarthritis dengan kondrosit daripada orang yang tidak mempunyai penyakit sendi, penulis memerhatikan perubahan ketara dalam pembebasan glikosaminoglikan oleh tisu rawan biasa secara in vitro, tetapi tahap pelepasan sitokin kekal tidak berubah. G. Hilal et al. (1998) menunjukkan bahawa kultur osteoblas daripada tulang subkondral pesakit dengan osteoarthritis secara in vitro mempunyai metabolisme yang diubah - aktiviti sistem AP/plasmin dan tahap IGF-1 dalam sel ini meningkat. Pemerhatian CI Westacott et al. (1997) boleh dijelaskan dengan peningkatan dalam aktiviti protease dalam sel tulang subkondral.
Ia masih tidak diketahui sama ada perubahan dalam tulang subkondral memulakan osteoarthritis atau menyumbang kepada perkembangannya. DK Dedrick et al. (1993) menunjukkan bahawa pada anjing dengan osteoarthritis akibat pembedahan, penebalan tulang subkondral bukanlah syarat yang diperlukan untuk perkembangan perubahan seperti osteoarthrosis dalam rawan artikular, tetapi menyumbang kepada perkembangan proses degeneratif dalam rawan. Hasil kajian oleh A. Sa'ied et al. (1997) bercanggah dengan data kajian lepas. Menggunakan echography 50 MHz untuk menilai perubahan morfologi awal dan perkembangannya dalam rawan artikular dan tulang dalam osteoarthritis eksperimen yang disebabkan oleh suntikan asid monoiodoacetic ke dalam sendi menyekat tikus, penulis menunjukkan proses serentak perubahan dalam tulang dan rawan semasa tiga hari pertama selepas suntikan.
Osteoblas merembeskan faktor pertumbuhan dan sitokin yang terlibat dalam pembentukan semula tulang tempatan, yang mungkin menggalakkan pembentukan semula rawan yang betul dalam sendi "menahan berat" selepas penembusannya melalui retakan mikro dalam lapisan rawan artikular yang terkalsifikasi. Selain itu, produk rembesan sel tulang terdapat dalam cecair sinovial. Produk yang paling berkemungkinan dirembes oleh osteoblas abnormal yang boleh memulakan proses pembentukan semula rawan tempatan ialah TGF-b dan protein morfometrik tulang (BMP). Kedua-dua ahli keluarga TGF dirembeskan oleh kedua-dua kondrosit dan osteoblas, dan kedua-duanya mampu mengubah suai pembentukan semula tulang dan rawan. J. Martel Pelletier et al. (1997) memerhatikan peningkatan dalam tahap TGF-β dalam eksplan tulang subkondral pesakit dengan osteoarthrosis berbanding individu yang sihat, yang menunjukkan kemungkinan peranan faktor pertumbuhan ini dalam patogenesis osteoarthrosis. IGF juga dihasilkan oleh osteoblas. Dalam budaya sel seperti osteoblas yang diperoleh daripada pesakit dengan osteoarthrosis, peningkatan tahap IGF didapati, yang mengubah metabolisme rawan.
TGF-b, IGF, BMP dan sitokin yang dihasilkan oleh osteoblas dalam tulang subkondral boleh mempengaruhi penghasilan kolagenase dan enzim proteolitik lain dalam rawan, yang seterusnya boleh menggalakkan pembentukan semula/degradasi matriks rawan. Masih tidak jelas sama ada osteoblas dalam OA menghasilkan kurang faktor perangsang koloni makrofaj (M-CSF - perangsang penyerapan tulang) berbanding sel normal. Hasil kajian oleh AG Uitterlinden et al. (1997) menunjukkan bahawa reseptor vitamin D, yang dinyatakan oleh osteoblas dan mengawal ekspresi beberapa faktor yang disintesis oleh sel-sel ini, mungkin memainkan peranan tertentu dalam pembentukan osteofit, yang sebahagiannya menerangkan peranan osteoblas dalam patogenesis penyakit ini.
Dengan mengambil kira hasil kajian di atas, G. Hilal et al. (1998), J. Martel-Pelletier et al. (1997) mencadangkan hipotesis kerja berikut tentang hubungan antara pembentukan semula tulang subkondral dan rawan artikular yang betul dalam osteoarthrosis. Pada peringkat awal atau peringkat lanjut patogenesis OA, proses pembentukan semula tisu tulang dalam tulang subkondral semakin meningkat. Pada masa yang sama, pemuatan berulang membawa kepada patah mikro tempatan dan/atau kemunculan ketidakseimbangan dalam sistem protein pengikat IGF/IGF (IGFBP) akibat tindak balas abnormal osteoblas tulang subkondral, yang menyumbang kepada sklerosisnya. Yang terakhir ini seterusnya boleh menyumbang kepada penampilan patah mikro rawan yang betul dan kerosakan pada matriksnya.
Di bawah keadaan biasa, kerosakan ini diperbaiki oleh sintesis tempatan dan pembebasan protein pengikat IGF-1 dan IGF, yang merangsang pembentukan ECM rawan artikular. Pada masa yang sama, sistem GF menggalakkan pertumbuhan sel tulang subkondral dan pembentukan matriks tulang. Aktiviti anabolik sistem IGF meningkat dalam tulang subkondral pesakit dengan osteoarthrosis, manakala pengaktifan tempatan sistem AP/plasmin (pengatur tempatan sistem IGF) dalam rawan artikular menyebabkan perubahan setempatnya. Dalam osteoblas dalam osteoarthrosis, IGF-1 mengganggu peraturan AP oleh plasmin oleh jenis maklum balas positif, oleh itu, ia boleh menghalang pembentukan semula dalam tisu tulang, yang akhirnya membawa kepada sklerosis subkondral. Oleh itu, dalam tisu tulang dan rawan, induksi tempatan IGF-1 dan protease membawa, di satu pihak, kepada kerosakan rawan, sebaliknya, kepada penebalan tulang subkondral, yang kedua seterusnya menyumbang kepada kerosakan rawan selanjutnya. Ketidakseimbangan antara kerosakan rawan yang berkaitan dengan sklerosis subkondral dan keupayaan reparatifnya membawa kepada perubahan progresif dalam ECM rawan dan kepada perkembangan osteoarthrosis. Menurut pengarang, hipotesis ini juga menerangkan perkembangan perlahan penyakit ini.

