Pakar perubatan artikel itu
Penerbitan baru
Virus kekurangan imun manusia (HIV)
Ulasan terakhir: 04.07.2025

Semua kandungan iLive disemak secara perubatan atau fakta diperiksa untuk memastikan ketepatan faktual sebanyak mungkin.
Kami mempunyai garis panduan sumber yang ketat dan hanya memautkan ke tapak media yang bereputasi, institusi penyelidikan akademik dan, apabila mungkin, dikaji semula kajian secara medis. Perhatikan bahawa nombor dalam kurungan ([1], [2], dan lain-lain) boleh diklik pautan ke kajian ini.
Jika anda merasakan bahawa mana-mana kandungan kami tidak tepat, ketinggalan zaman, atau tidak dipersoalkan, sila pilih dan tekan Ctrl + Enter.
Sindrom kekurangan imun yang diperoleh telah dikenal pasti sebagai penyakit khusus pada tahun 1981 di Amerika Syarikat, apabila sebilangan orang muda mengalami penyakit serius yang disebabkan oleh mikroorganisma yang tidak patogenik atau patogenik yang lemah untuk orang yang sihat. Kajian tentang status imun pesakit menunjukkan penurunan mendadak dalam bilangan limfosit secara umum dan T-helper khususnya. Keadaan ini dipanggil AIDS (Acquired Immune Deficiency Syndrome). Kaedah jangkitan (hubungan seksual, melalui darah dan persediaannya) menunjukkan sifat berjangkit penyakit.
Agen penyebab AIDS ditemui pada tahun 1983 secara bebas oleh orang Perancis L. Montagnier, yang memanggilnya LAV Lymphoadenopathy Associated Virus, kerana dia menemuinya pada pesakit dengan limfadenopati; dan R. Gallo Amerika, yang menamakan virus itu HTLV-III (Human T-limfotropik Virus III): dia sebelum ini telah menemui virus limfotropik I dan II.
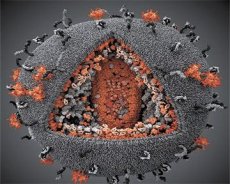
Perbandingan sifat-sifat virus LAV dan HTLV-III menunjukkan identiti mereka, jadi untuk mengelakkan kekeliruan, virus itu dinamakan HIV (Human Immunodeficiency Virus, atau HIV) pada tahun 1986. HIV berbentuk sfera, dengan diameter 110 nm. Sampul virus mempunyai bentuk polihedron, terdiri daripada 12 pentagon dan 20 heksagon. Di tengah dan sudut setiap heksagon adalah molekul protein glikosilasi gpl20 (nombor 120 menunjukkan berat molekul protein dalam kilodalton). Sejumlah 72 molekul gpl20 terletak di permukaan virion dalam bentuk pancang yang aneh, setiap satunya dikaitkan dengan protein intramembran gp41. Protein ini, bersama dengan lapisan lipid berganda, membentuk superkapsid (membran) virion.
Protein gpl20 dan gp41 dibentuk dengan memotong protein prekursor Env oleh protease selular. Protein gp41 membentuk "batang" spike dengan mengikat dengan domain sitoplasmanya ke protein matriks p17MA yang terletak terus di bawah sampul surat. Molekul p17 berinteraksi semasa pematangan virion untuk membentuk ikosahedron yang mendasari sampul surat.
Di bahagian tengah virion, protein p24 membentuk kapsid berbentuk kon. Bahagian kapsid yang sempit disambungkan ke membran virion dengan penyertaan protein rb. Di dalam kapsid, terdapat dua molekul RNA genomik virus yang sama. Mereka disambungkan oleh hujung 5' mereka kepada protein nukleokapsid p7NC. Protein ini menarik kerana ia mempunyai dua residu asid amino (motif) yang kaya dengan sistein dan histidin dan mengandungi atom Zn - ia dipanggil "jari zink" kerana ia menangkap molekul RNA genomik untuk dimasukkan ke dalam virion yang membentuk. Kapsid juga mengandungi tiga enzim. Revertase (RT), atau kompleks pol, termasuk transkripase terbalik, RNase H dan polimerase DNA yang bergantung kepada DNA. Revertase hadir sebagai heterodimer p66/p51. Protease (PR) - p10, memulakan dan melaksanakan proses pematangan virion. Integrase (IN) - p31, atau endonuclease, memastikan kemasukan DNA proviral ke dalam genom sel perumah. Kapsid juga mengandungi molekul RNA primer (tRNAl"3).
Genom RNA dalam sel ditukar kepada genom DNA (DNA provirus) dengan bantuan transkripase terbalik, yang terdiri daripada 9283 pasangan nukleotida. Ia bersempadan di kiri dan kanan dengan apa yang dipanggil ulangan terminal panjang, atau LTR: S'-LTR di sebelah kiri dan 3'-LTR di sebelah kanan. LTR mengandungi 638 pasangan nukleotida setiap satu.
Genom HIV terdiri daripada 9 gen, beberapa daripadanya bertindih di hujung (mempunyai beberapa bingkai bacaan) dan mempunyai struktur eksonintron. Mereka mengawal sintesis 9 struktur dan 6 protein pengawalseliaan.
Kepentingan LTR untuk genom virus ialah ia mengandungi unsur kawal selia berikut yang mengawal fungsinya:
- isyarat transkripsi (rantau promoter);
- isyarat tambahan poli-A;
- isyarat capping;
- isyarat integrasi;
- isyarat peraturan positif (TAR untuk protein TAT);
- unsur pengawalseliaan negatif (NRE untuk protein NEF);
- tapak untuk lampiran RNA primer (tRNA™3) untuk sintesis DNA untai tolak pada hujung 3'; isyarat di hujung 5' LTR yang berfungsi sebagai primer untuk sintesis DNA untai tambah.
Selain itu, LTR mengandungi unsur-unsur yang terlibat dalam pengawalan penyambungan mRNA, pembungkusan molekul vRNA ke dalam kapsid (unsur Psi). Akhirnya, semasa transkripsi genom, dua isyarat terbentuk dalam mRNA panjang untuk protein REV, yang menukar sintesis protein: CAR - untuk protein pengawalseliaan dan CRS - untuk protein struktur. Jika protein REV mengikat CAR, protein struktur disintesis; jika ia tiada, hanya protein pengawalseliaan yang disintesis.
Gen pengawalseliaan berikut dan proteinnya memainkan peranan yang sangat penting dalam mengawal fungsi genom virus:
- Protein TAT, yang menjalankan kawalan positif replikasi virus dan bertindak melalui kawasan kawal selia TAR;
- Protein NEV dan VPU, yang menggunakan kawalan negatif replikasi melalui rantau NRE;
- Protein REV, yang menjalankan kawalan positif-negatif. Protein REV mengawal kerja gen gag, pol, env dan menjalankan peraturan negatif penyambungan.
Oleh itu, replikasi HIV berada di bawah kawalan tiga kali ganda - positif, negatif dan positif-negatif.
Protein VIF menentukan kejangkitan virus yang baru disintesis. Ia dikaitkan dengan protein kapsid p24 dan terdapat dalam virion dalam jumlah 60 molekul. Protein NEF diwakili dalam virion oleh sebilangan kecil molekul (5-10), mungkin dikaitkan dengan sampul surat.
Protein VPR menghalang kitaran sel pada fasa G2, mengambil bahagian dalam pengangkutan kompleks praintegrasi ke dalam nukleus sel, mengaktifkan beberapa gen virus dan selular, dan meningkatkan kecekapan replikasi virus dalam monosit dan makrofaj. Lokasi protein VPR, TAT, REV, dan VPU dalam virion belum ditetapkan.
Sebagai tambahan kepada proteinnya sendiri, membran virion mungkin mengandungi beberapa protein sel perumah. Protein VPU dan VPR mengambil bahagian dalam peraturan pembiakan virus.
Varian antigenik human immunodeficiency virus (HIV)
Virus immunodeficiency manusia (HIV) sangat berubah-ubah. Walaupun dari badan seorang pesakit, strain virus boleh diasingkan yang berbeza dengan ketara dalam sifat antigen. Kebolehubahan sedemikian dipermudahkan oleh pemusnahan intensif sel CD4+ dan tindak balas antibodi yang kuat terhadap jangkitan HIV. Satu bentuk HIV baru, HIV-2, secara biologi hampir dengan HIV-1 tetapi secara imunologi berbeza daripadanya, telah diasingkan daripada pesakit dari Afrika Barat. Homologi struktur utama genom virus ini ialah 42%. Provirus DNA HIV-2 mengandungi 9671 bp, dan LTRnya - 854 bp. HIV-2 kemudiannya diasingkan di kawasan lain di dunia. Tiada imuniti silang antara HIV-1 dan HIV-2. Dua bentuk besar HIV-1 diketahui: O (Outlier) dan M (Major), yang kedua dibahagikan kepada 10 subjenis (AJ). Lapan subtipe (AH) beredar di Rusia.
 [ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
[ 1 ], [ 2 ], [ 3 ], [ 4 ], [ 5 ], [ 6 ], [ 7 ], [ 8 ], [ 9 ], [ 10 ]
Mekanisme interaksi HIV dengan sel
Setelah menembusi badan, virus mula-mula menyerang sel yang mengandungi reseptor CD4 khusus untuknya. Reseptor ini terdapat dalam kuantiti yang banyak dalam T-helper, dalam kuantiti yang lebih kecil dalam makrofaj dan monosit, dan T-helpers sangat sensitif terhadap virus.
Human immunodeficiency virus (HIV) mengiktiraf reseptor CD4 menggunakan protein gpl20nya. Proses interaksi HIV dengan sel berlaku mengikut skema berikut: penjerapan pengantara reseptor -> lubang bersalut -> vesikel bersalut -> lisosom. Di dalamnya, membran virion bersatu dengan membran lisosom, dan nukleokapsid, dibebaskan daripada superkapsid, memasuki sitoplasma; dalam perjalanan ke nukleus, ia dimusnahkan, dan RNA genom dan komponen teras yang berkaitan dikeluarkan. Kemudian, transkripase terbalik mensintesis untaian tolak DNA pada RNA virion, kemudian RNase H memusnahkan RNA virion, dan polimerase DNA virus mensintesis untaian tambah DNA. 5'-LTR dan 3'-LTR terbentuk di hujung provirus DNA. Provirus DNA boleh kekal dalam nukleus untuk beberapa waktu dalam bentuk tidak aktif, tetapi lambat laun ia disepadukan ke dalam kromosom sel sasaran dengan bantuan integrasenya. Di dalamnya, provirus kekal tidak aktif sehingga T-limfosit yang diberikan diaktifkan oleh antigen mikrob atau sel imunokompeten lain. Pengaktifan transkripsi DNA selular dikawal oleh faktor nuklear khas (NF-kB). Ia adalah protein pengikat DNA dan dihasilkan dalam kuantiti yang banyak semasa pengaktifan dan percambahan T-limfosit dan monosit. Protein ini mengikat urutan tertentu DNA selular dan urutan LTR serupa provirus DNA dan mendorong transkripsi kedua-dua DNA selular dan provirus DNA. Dengan mendorong transkripsi provirus DNA, ia menjalankan peralihan virus daripada keadaan tidak aktif kepada yang aktif dan, dengan itu, daripada jangkitan berterusan kepada yang produktif. Provirus boleh kekal dalam keadaan tidak aktif untuk masa yang sangat lama. Pengaktifan virus adalah saat kritikal dalam interaksinya dengan sel.
Dari saat virus menembusi sel, tempoh jangkitan HIV bermula - keadaan pembawa virus, yang boleh bertahan 10 tahun atau lebih; dan dari saat virus itu diaktifkan, penyakit itu bermula - AIDS. Dengan bantuan gen pengawalseliaan dan produknya, virus mula membiak secara aktif. Protein TAT boleh meningkatkan kadar pembiakan virus sebanyak 1000 kali ganda. Transkripsi virus adalah kompleks. Ia termasuk pembentukan kedua-dua mRNA penuh dan subgenomik, penyambungan mRNA, dan kemudian sintesis protein struktur dan pengawalseliaan berlaku.
Sintesis protein struktur berlaku seperti berikut. Pertama, poliprotein prekursor Pr55Gag (protein dengan berat molekul 55 kDa) disintesis. Ia mengandungi 4 domain utama: matriks (MA), kapsid (CA), nukleokapsid (NC), dan domain rb, dari mana, sebagai hasil pemotongan Pr55Gag oleh protease virus (ia dipotong sendiri daripada protein prekursor lain, Gag-Pol), protein struktur p17, p24, p7, dan rb terbentuk, masing-masing. Pembentukan poliprotein Pr55Gag adalah syarat utama untuk pembentukan zarah virus. Protein inilah yang menentukan program morfogenesis virion. Ia secara berurutan merangkumi peringkat pengangkutan poliprotein Gag ke membran plasma, interaksi dengannya, dan interaksi protein-protein semasa pembentukan zarah virus dan tunasnya. Pr55Gag disintesis pada poliribosom bebas; Molekul protein diangkut ke membran, di mana ia berlabuh oleh kawasan hidrofobiknya. Domain CA memainkan peranan utama dalam mewujudkan konformasi asli protein Gag. Domain NC memastikan kemasukan (dengan bantuan "jari zink") 2 molekul RNA genomik dalam komposisi zarah virus yang membentuk. Molekul poliprotein pada mulanya dimerisasi disebabkan oleh interaksi domain matriks. Kemudian dimer bergabung menjadi kompleks heksamerik (daripada 6 unit) hasil daripada interaksi domain CA dan NC. Akhirnya, heksamer, bercantum pada permukaan sisinya, membentuk virion sfera yang tidak matang, di dalamnya terkandung RNA virus genomik, ditangkap oleh domain NC.
Satu lagi protein prekursor, Prl60Gag-Pol (protein dengan berat molekul 160 kDa), disintesis hasil daripada anjakan bingkai oleh ribosom semasa penterjemahan 3'-hujung gen gag di rantau yang terletak serta-merta di hulu rantau yang mengekod protein rb. Poliprotein Gag-Pol ini mengandungi jujukan protein Gag yang tidak lengkap (1-423 asid amino) dan jujukan Pol yang merangkumi domain PR, RT dan IN. Molekul poliprotein Gag-Pol juga disintesis pada poliribosom bebas dan diangkut ke membran plasma. Poliprotein Prl60Gagpol mengandungi semua tapak interaksi antara molekul dan tapak pengikat membran yang wujud dalam poliprotein Gag. Oleh itu, molekul poliprotein Gag-Pol bercantum dengan membran dan, bersama-sama dengan molekul Gag, termasuk dalam virion yang membentuk, menghasilkan penampilan protease aktif dan permulaan proses pematangan virion. Protease HIV-1 sangat aktif hanya dalam bentuk dimer, oleh itu, untuk pengasingan sendiri daripada Prl60Gag-Pol, dimerisasi molekul ini diperlukan. Pematangan virion terdiri daripada fakta bahawa protease aktif yang dikeluarkan memotong prl60Gag-Pol dan Gag55 di tapak yang diiktiraf olehnya; protein p17, p24, p7, p6, revertase, integrase terbentuk dan perkaitannya ke dalam struktur virus berlaku.
Protein Env disintesis pada ribosom yang dikaitkan dengan membran retikulum endoplasma, kemudian ia diglikosilasi, dipotong oleh protease selular menjadi gp120 dan gp41, dan diangkut ke permukaan sel. Dalam kes ini, gp41 menembusi membran dan mengikat kepada domain matriks molekul protein Gag yang dikaitkan dengan permukaan dalaman membran. Sambungan ini dipelihara dalam virion matang.
Oleh itu, pemasangan zarah virus terdiri daripada pengagregatan protein prekursor dan molekul RNA yang berkaitan pada membran plasma sel perumah, pembentukan virion yang tidak matang dan pembebasannya dengan tunas dari permukaan sel. Semasa tunas, virion mengelilingi dirinya dengan membran sel di mana molekul gp41 dan gp120 tertanam. Semasa tunas atau, mungkin, selepas pembebasan virion, kematangan mereka berlaku, yang dijalankan dengan bantuan protease virus dan terdiri daripada pemotongan proteolitik protein prekursor Pr55Gag dan Prl60Gag-Pol ke dalam protein virus matang dan persatuannya ke dalam kompleks struktur tertentu. Peranan utama dalam proses morfogenesis virus dimainkan oleh poliprotein prekursor Pr55Gag, yang mengatur dan memasang virion yang tidak matang; proses pematangannya diselesaikan oleh protease virus tertentu.
Punca kekurangan imun
Salah satu punca utama kekurangan imun dalam jangkitan HIV ialah kematian besar-besaran T-helpers. Ia berlaku akibat daripada peristiwa berikut. Pertama, T-helper yang dijangkiti virus mati akibat apoptosis. Adalah dipercayai bahawa dalam pesakit AIDS, replikasi virus, apoptosis, dan penurunan bilangan T-helper saling berkaitan. Kedua, T-pembunuh mengenali dan memusnahkan sel-T yang dijangkiti virus atau membawa molekul gpl20 yang terserap, serta T-helper yang dijangkiti virus dan tidak dijangkiti virus, yang membentuk simplas (syncytium) yang terdiri daripada beberapa dozen sel (sesetengahnya mati akibat pembiakan virus di dalamnya). Akibat pemusnahan sejumlah besar T-helper, terdapat penurunan dalam ekspresi reseptor membran dalam B-limfosit kepada interleukin-2, sintesis pelbagai interleukin (faktor pertumbuhan dan pembezaan B-limfosit - IL-4, IL-5, IL-6, dsb.) mengganggu fungsi sistem T, mengakibatkan gangguan sistem. Aktiviti sistem pelengkap dan makrofaj ditindas. Makrofaj dan monosit yang dijangkiti virus tidak mati untuk masa yang lama, tetapi mereka tidak dapat mengeluarkan virus dari badan. Akhirnya, disebabkan persamaan struktur dan antigen gpl20 dengan reseptor beberapa sel epitelium badan (termasuk reseptor trofoblas yang menjadi pengantara penghantaran pemindahan HIV), antibodi antireseptor dengan spektrum tindakan yang luas disintesis. Antibodi sedemikian mampu menyekat pelbagai reseptor selular dan merumitkan perjalanan penyakit dengan gangguan autoimun. Akibat jangkitan HIV adalah kekalahan semua pautan utama sistem imun. Pesakit sedemikian menjadi tidak berdaya melawan pelbagai jenis mikroorganisma. Ini membawa kepada perkembangan jangkitan dan tumor oportunistik. Bagi pesakit yang dijangkiti HIV, risiko mendapat sekurang-kurangnya tiga jenis kanser meningkat: sarkoma Kaposi; karsinoma (termasuk kanser kulit); Limfoma sel B, yang berlaku disebabkan oleh transformasi malignan B-limfosit. Walau bagaimanapun, HIV bukan sahaja limfositotropik, tetapi juga neurotropik. Ia menembusi ke dalam sel-sel sistem saraf pusat (astrocytes) kedua-dua oleh endositosis pengantara reseptor dan oleh fagositosis limfoblas yang dijangkiti virus oleh astrocytes. Apabila virus berinteraksi dengan astrosit, simplas juga terbentuk, yang memudahkan penyebaran patogen melalui saluran antara sel. Virus ini boleh bertahan dalam makrofaj dan monosit untuk masa yang lama, jadi ia berfungsi sebagai takungan dan pengedarnya di dalam badan, dapat menembusi semua tisu. Makrofaj yang dijangkiti memainkan peranan utama dalam pengenalan HIV ke dalam sistem saraf pusat dan kerosakannya. Dalam 10% pesakit, sindrom klinikal primer dikaitkan dengan kerosakan pada sistem saraf pusat dan nyata sebagai demensia. Oleh itu, orang yang dijangkiti HIV dicirikan oleh 3 kumpulan penyakit - jangkitan oportunistik,penyakit tumor dan kerosakan pada sistem saraf pusat.
Epidemiologi jangkitan HIV
Sumber jangkitan HIV hanya seseorang - orang yang sakit atau pembawa virus. Virus immunodeficiency manusia (HIV) terkandung dalam darah, sperma, cecair serviks; dalam ibu yang menyusu - dalam susu ibu. Jangkitan berlaku secara seksual, melalui darah dan persediaannya, serta dari ibu kepada anak sebelum, semasa dan selepas bersalin. Kes jangkitan virus melalui makanan, minuman dan gigitan serangga tidak diketahui.
Ketagihan dadah menyumbang kepada penyebaran AIDS. Insiden HIV semakin meningkat setiap tahun. Menurut WHO, dari 1980 hingga 2000, 58 juta orang telah dijangkiti HIV. Pada tahun 2000 sahaja, 5.3 juta orang telah dijangkiti di seluruh dunia, dan 3 juta orang mati akibat AIDS. Sehingga 1 Januari 2004, 264 ribu orang yang dijangkiti HIV telah didaftarkan di Rusia. Separuh daripada orang yang dijangkiti HIV mati dalam tempoh 11-12 tahun dari saat jangkitan. Pada awal tahun 2004, daripada setiap 100 ribu rakyat Rusia, kira-kira 180 hidup dengan diagnosis "jangkitan HIV". Diramalkan bahawa dengan tahap morbiditi ini, jumlah orang yang dijangkiti HIV di Rusia menjelang 2012 akan menjadi 2.5-3 juta orang. Kerumitan memerangi jangkitan HIV bergantung kepada beberapa sebab: pertama, tiada kaedah yang berkesan untuk rawatan dan pencegahan khusus; Kedua, tempoh inkubasi untuk jangkitan HIV boleh melebihi 10 tahun. Tempohnya bergantung pada saat pengaktifan T-limfosit dan provirus DNA yang terkandung dalam kromosomnya. Masih tidak jelas sama ada semua orang yang dijangkiti virus itu ditakdirkan untuk AIDS atau sama ada penghantaran jangka panjang virus tanpa penyakit adalah mungkin (yang nampaknya tidak mungkin). Akhirnya, terdapat beberapa virus kekurangan imun manusia (HIV-1, HIV-2), perbezaan antigen di antaranya menghalang pembentukan imuniti silang. Penemuan virus immunodeficiency simian (SIV) menjelaskan persoalan asal usul HIV. SIV adalah serupa dengan HIV dalam organisasi genomnya, tetapi berbeza dengan ketara dalam jujukan nukleotidanya. HIV-2 menduduki kedudukan pertengahan antara HIV-1 dan SIV dalam sifat serologinya, dan lebih dekat dengan SIV dalam jujukan nukleotidanya. Dalam hal ini, VM Zhdanov mencadangkan bahawa virus HIV-1, HIV-2 dan SIV berasal daripada nenek moyang yang sama. Ada kemungkinan, menurut R. Gallo, bahawa salah satu SIV entah bagaimana memasuki tubuh manusia, di mana ia mengalami beberapa siri mutasi, mengakibatkan kemunculan HIV-1, HIV-2 dan bentuk lain.
Gejala jangkitan HIV
Virus immunodeficiency manusia mempunyai beberapa ciri yang sebahagian besarnya menentukan patogenesis penyakit. Virus ini mempunyai kadar pembiakan yang sangat tinggi, ditentukan oleh unsur pengawalseliaannya (sehingga 5,000 virion disintesis dalam 5 minit dalam peringkat aktif). Disebabkan kehadiran protein gabungan (gp41), virus mendorong pembentukan struktur syncytial yang luas akibat gabungan T-helper yang dijangkiti dan tidak dijangkiti, yang mengakibatkan kematian besar-besaran mereka. Molekul protein gpl20 yang terbentuk dalam kuantiti yang banyak beredar bebas dalam darah dan terikat pada reseptor T-helpers yang tidak dijangkiti, akibatnya ia juga dikenali dan dimusnahkan oleh T-killers. Virus ini boleh merebak melalui saluran antara sel dari sel ke sel, dalam hal ini ia menjadi sukar diakses oleh antibodi.
Kriteria klinikal untuk jangkitan HIV
Pada orang dewasa, jangkitan HIV didiagnosis apabila mereka mempunyai sekurang-kurangnya dua simptom serius dalam kombinasi dengan sekurang-kurangnya satu simptom kecil dan tanpa ketiadaan punca kekurangan imun yang lain (kanser, kekurangan imun kongenital, kebuluran teruk, dsb.). Gejala serius termasuk:
- penurunan berat badan sebanyak 10% atau lebih;
- keadaan demam yang berpanjangan, terputus-putus atau berterusan;
- cirit-birit kronik.
Gejala kecil: batuk berterusan, dermatitis umum, herpes zoster berulang, kandidiasis oral dan pharyngeal, herpes simplex kronik, limfadenopati umum. Diagnosis AIDS dibuat dengan kehadiran hanya sarkoma Kaposi, meningitis kriptokokus, pneumonia pneumocystis. Gambar klinikal penyakit ini dipengaruhi oleh jangkitan oportunistik yang disertakan.
Kaedah pembiakan virus kekurangan imun manusia (HIV)
HIV-1 dan HIV-2 boleh ditanam dalam sel hanya satu klon limfosit TCV4 - H9, diperoleh daripada limfosit TCV4 leukemik. Kultur monolayer sel astrosit, di mana HIV-1 membiak dengan baik, juga boleh digunakan untuk tujuan ini. Cimpanzi terdedah kepada HIV-1 di kalangan haiwan.
Rintangan virus dalam persekitaran luaran adalah rendah. Ia mati di bawah pengaruh cahaya matahari dan sinaran UV, dimusnahkan pada 80 °C dalam masa 30 minit, apabila dirawat dengan disinfektan yang biasa digunakan - dalam masa 20-30 minit. Untuk membasmi kuman bahan yang mengandungi virus, perlu menggunakan disinfektan mikobakterisida, kerana ia berkesan terhadap mikroorganisma dengan rintangan tertinggi.
Diagnosis makmal jangkitan HIV
Kaedah utama untuk mendiagnosis pengangkutan virus dan jangkitan HIV ialah enzim immunoassay. Walau bagaimanapun, disebabkan fakta bahawa gpl20 mempunyai persamaan struktur dan antigen dengan reseptor beberapa sel manusia, termasuk reseptor yang mengangkut imunoglobulin melalui sel epitelium membran mukus, antibodi yang berkaitan dengan antibodi terhadap gpl20 mungkin muncul di dalam badan. Dalam kes ini, mungkin terdapat hasil ELISA positif palsu. Oleh itu, semua sera yang bertindak balas positif daripada subjek menjalani analisis tambahan menggunakan kaedah immunoblotting, atau Western blotting. Kaedah ini adalah berdasarkan pengenalpastian antibodi yang dikaji selepas pemisahan elektroforesis dan ujian seterusnya menggunakan antibodi anti-spesies berlabel. Kaedah virologi jarang digunakan kerana kerumitan pembiakan virus. Klon limfosit H9 digunakan untuk mendapatkan antigen virus - komponen sistem ujian diagnostik yang diperlukan. Kaedah CPR membolehkan pengesanan virus pada peringkat awal viremia.
Rawatan jangkitan HIV
Ia adalah perlu untuk mencari atau mensintesis ubat-ubatan yang berkesan menyekat aktiviti transkripase terbalik (revertase) atau protease virus. Mereka akan menghalang pembentukan provirus DNA dan (atau) menghalang pembiakan intraselular virus. Strategi moden untuk merawat pesakit yang dijangkiti HIV adalah berdasarkan prinsip penggunaan gabungan ubat yang menghalang protease virus (salah satu ubat) dan terbalik (2 ubat berbeza) - terapi gabungan (tiga kali ganda). Di Rusia, untuk rawatan pesakit yang dijangkiti HIV, penggunaan gabungan 2 ubat domestik disyorkan: fosfazide dan crixivan, yang secara khusus menyekat pembiakan HIV pada peringkat awal dan akhir pembiakan, terutamanya dengan pengurangan aktiviti azidothymidine.
Masalah profilaksis khusus adalah keperluan untuk mencipta vaksin yang akan memastikan pembentukan imuniti pengantara sel yang berkesan berdasarkan limfosit sitotoksik khusus virus tanpa sebarang pengeluaran antibodi yang ketara. Kekebalan sedemikian disediakan oleh pembantu Thl. Ada kemungkinan bahawa antibodi, termasuk yang meneutralkan virus, bukan sahaja tidak berkesan dalam menyekat jangkitan HIV, tetapi pada tahap yang tinggi ia menekan imuniti yang dimediasi sel. Oleh itu, vaksin anti-HIV mesti memenuhi, pertama sekali, dua keperluan utama: a) benar-benar selamat dan b) merangsang aktiviti limfosit T-sitotoksik. Keberkesanan pelbagai varian vaksin yang diperoleh daripada virus yang dibunuh (tidak aktif) dan daripada antigen individu dengan sifat perlindungan yang tinggi sedang dikaji. Antigen tersebut sama ada boleh diasingkan daripada virion itu sendiri atau disintesis secara kimia. Vaksin yang dicipta berdasarkan kaedah kejuruteraan genetik telah dicadangkan. Ia adalah virus vaccinia rekombinan yang membawa gen HIV yang bertanggungjawab untuk sintesis antigen dengan sifat imunogenik yang kuat. Persoalan keberkesanan vaksin ini memerlukan masa yang agak lama kerana tempoh inkubasi jangkitan HIV yang panjang dan kebolehubahan patogen yang tinggi. Penciptaan vaksin yang sangat berkesan terhadap HIV adalah masalah asas yang mendesak.

